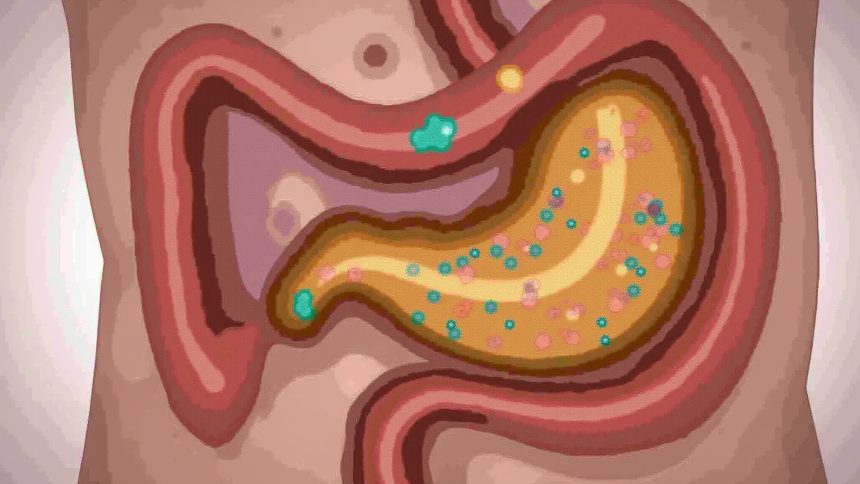
A gyomorsav, vagy sósav (HCl), nélkülözhetetlen szerepet játszik az emésztési folyamatokban. A gyomorban termelődve felelős a táplálék lebontásáért, különösen a fehérjék denaturálásáért, ami elősegíti a pepsin enzim hatékony működését. Emellett a gyomorsav antimikrobiális hatással is bír, elpusztítva a táplálékkal bekerülő kórokozókat, védve ezzel a szervezetet a fertőzésektől. A megfelelő gyomorsavszint tehát elengedhetetlen a tápanyagok felszívódásához és az egészség megőrzéséhez.
A gyomorsav termelésének kulcsfontosságú szereplője a protonpumpa (H+/K+ ATPáz). Ez a fehérje található meg a gyomor parietális sejtjeinek membránjában. Működése során aktívan szállítja a hidrogénionokat (H+) a gyomor üregébe, cserébe káliumionokért (K+). Ez az ioncsere hozza létre a gyomorban a rendkívül savas környezetet.
A protonpumpa tehát a gyomorsav termelésének központi eleme, nélküle a gyomor nem lenne képes a megfelelő savasság elérésére, ami elengedhetetlen az emésztéshez és a kórokozók elleni védekezéshez.
A protonpumpa működését különböző tényezők szabályozzák, beleértve a hormonszintet (pl. gasztrin), a neurotranszmittereket (pl. acetilkolin) és a hisztamint. Ezek a szabályozó mechanizmusok biztosítják, hogy a gyomorsav termelése a szervezet igényeihez igazodjon. A protonpumpa gátlók (PPI-k) olyan gyógyszerek, amelyek specifikusan gátolják a protonpumpa működését, csökkentve ezzel a gyomorsav termelést. Ezek a gyógyszerek széles körben alkalmazottak a gyomorsav túlzott termelése által okozott betegségek kezelésére, mint például a reflux vagy a gyomorfekély.
A gyomor anatómiája és a gyomorsav termelés helyszíne
A gyomor egy J alakú, tágulékony szerv, amely a nyelőcső és a vékonybél között helyezkedik el. Funkciója összetett: tárolja a lenyelt ételt, megkezdi a fehérjék emésztését, és szabályozza a táplálék továbbjutását a vékonybélbe. Anatómiailag több részre osztható: a cardia (a nyelőcsőhöz csatlakozó rész), a fundus (a cardia felett elhelyezkedő kupolaszerű rész), a corpus (a gyomor fő része) és az antrum (a gyomor alsó, a patkóbélhez csatlakozó része).
A gyomorsav termelése elsősorban a gyomor falában található speciális sejtek, a parietális sejtek (más néven fedősejtek) feladata. Ezek a sejtek legfőképpen a corpusban és a fundusban koncentrálódnak. A gyomor nyálkahártyája számos apró gödröcskét tartalmaz, ezek a gyomormirigyek bejáratai. A gyomormirigyek különböző sejttípusokat tartalmaznak, amelyek különböző anyagokat termelnek, például gyomorsavat, pepszinogént (egy enzim előanyaga) és nyákot.
A parietális sejtek bonyolult módon állítják elő a gyomorsavat (sósavat, HCl). A folyamat során a sejtek citoplazmájában szén-dioxidból és vízből szénsav képződik, mely disszociál hidrogénionokra (H+) és bikarbonátionokra (HCO3–). A hidrogénionok aktív transzporttal kerülnek a gyomor lumenébe, a parietális sejt membránjában található H+/K+ ATP-áz, vagyis a protonpumpa segítségével. Ez a pumpa a hidrogénionokat a gyomor üregébe pumpálja, miközben káliumionokat (K+) szállít vissza a sejtbe. A bikarbonátionok a véráramba kerülnek, ami ideiglenesen megnöveli a vér pH-ját (ezt nevezik „alkáli dagálynak”).
Fontos megjegyezni, hogy a gyomorban más sejtek is fontos szerepet játszanak az emésztésben. A fősejtek pepszinogént termelnek, amely a savas környezetben pepszinné alakulva fehérjéket bont. A nyáktermelő sejtek védőréteget képeznek a gyomor falán, megakadályozva, hogy a sav károsítsa azt. Emellett a G-sejtek gasztrint termelnek, egy hormont, amely serkenti a parietális sejtek savtermelését.
A parietális sejtekben található protonpumpa (H+/K+ ATP-áz) kulcsfontosságú a gyomorsav termelésében, mivel ez a mechanizmus teszi lehetővé a hidrogénionoknak a gyomor lumenébe történő aktív transzportját, ami elengedhetetlen a gyomorsav megfelelő koncentrációjának fenntartásához.
A gyomorsav termelését többféle tényező befolyásolja, többek között a táplálék összetétele, a vegetatív idegrendszer és különböző hormonok. A savtermelés szabályozása bonyolult folyamat, amelynek célja a hatékony emésztés biztosítása és a gyomor védelme.
A gyomor parietális sejtjeinek szerkezete és funkciója
A gyomor parietális sejtjei, más néven fedősejtek, a gyomor mirigyeiben találhatók, és kulcsfontosságú szerepet játszanak a gyomorsav (sósav, HCl) termelésében. Ezek a sejtek jellegzetes morfológiával rendelkeznek, ami lehetővé teszi a hatékony savszekréciót.
A parietális sejtek fő jellemzője a kiterjedt intracelluláris canalicularis rendszer, amely egy bonyolult membránredő-hálózat a sejt apikális felszínén. Ez a rendszer jelentősen megnöveli a sejt felszínét, ami elengedhetetlen a nagy mennyiségű sósav szekréciójához. A membránokban található a H+/K+-ATPáz, közismertebb nevén a protonpumpa.
A parietális sejtek citoplazmájában rengeteg mitokondrium található. Ez azért van, mert a protonpumpa működése energiaigényes folyamat, melyhez az ATP-t (adenozin-trifoszfát) a mitokondriumok biztosítják. A mitokondriumok tehát a sejtek „erőműveiként” funkcionálnak.
A parietális sejtek működése szigorú szabályozás alatt áll, melyet különböző hormonok és neurotranszmitterek befolyásolnak. Ilyen például a hisztamin, az acetilkolin és a gasztrin. Ezek a molekulák specifikus receptorokhoz kötődve serkentik a protonpumpa aktivitását és ezáltal a savtermelést.
A protonpumpa a parietális sejt apikális membránjában található transzmembrán fehérje, mely aktívan pumpálja a hidrogénionokat (H+) a gyomor lumenébe, a káliumionok (K+) cseréjével. Ez a folyamat hozza létre a gyomorsavat.
A savtermeléshez szükséges kloridionok (Cl–) a parietális sejt basolaterális membránján keresztül jutnak be a sejtbe, majd a canalicularis rendszeren keresztül távoznak a gyomor lumenébe. A hidrogénionok és kloridionok találkozása a gyomor üregében eredményezi a sósav (HCl) képződését.
A parietális sejtek nem csupán a sósavat termelik, hanem az intrinsic faktort is, ami a B12-vitamin felszívódásához elengedhetetlen. Ennek hiánya vérszegénységhez (pernicious anaemia) vezethet.
A protonpumpa (H+/K+ ATPáz) részletes leírása: szerkezet, alegységek és működési mechanizmus
A gyomor parietális sejtjeinek apikális membránjában található H+/K+ ATPáz, közismertebb nevén protonpumpa, kulcsfontosságú szerepet játszik a gyomorsav, azaz a sósav (HCl) termelésében. Ez az enzim felelős a hidrogénionok (H+) aktív transzportjáért a parietális sejtek citoplazmájából a gyomor lumenjébe, miközben káliumionokat (K+) szállít vissza a lumenből a sejtbe. Ez a folyamat a gyomor savas pH-jának fenntartásához elengedhetetlen.
A protonpumpa egy integráns membránfehérje, amely két fő alegységből áll: az α (alfa) és a β (béta) alegységből. Az α alegység (körülbelül 100 kDa) katalitikus funkciót lát el; ezen található az ATP kötőhely, a foszforilációs hely és a iontranszport csatorna. A β alegység (körülbelül 60-90 kDa) a fehérje megfelelő konformációjának kialakításában és stabilizálásában, valamint a sejtfelszínre való szállításában játszik szerepet. Mindkét alegység nélkülözhetetlen a protonpumpa helyes működéséhez.
A működési mechanizmus során az ATP hidrolízise által felszabaduló energia hajtja a H+ ionok transzportját a koncentrációgradiens ellenében. A folyamat ciklikusan zajlik, különböző konformációs állapotokon keresztül.
- E1 állapot: A pumpa a citoplazma felé néz, és nagy affinitással kötődik a H+ ionokhoz.
- E1~P állapot: Az ATP kötődése és hidrolízise foszforilálja a pumpát, ami konformációs változást idéz elő.
- E2~P állapot: A pumpa a gyomor lumenje felé néz, és csökken az affinitása a H+ ionokhoz, így azok felszabadulnak a lumenbe. Ezzel egyidejűleg a K+ ionok kötődnek a pumpához.
- E2 állapot: A defoszforiláció visszaállítja a pumpát az eredeti E1 állapotba, miközben a K+ ionok a citoplazmába jutnak.
Ez a ciklus ismétlődik, folyamatosan pumpálva a H+ ionokat a gyomor lumenjébe, és fenntartva a savas környezetet. A protonpumpa aktivitását különböző tényezők szabályozzák, beleértve a hormonális (pl. hisztamin, gasztrin) és idegi (pl. vagus ideg) hatásokat. Ezek a szabályozó mechanizmusok biztosítják, hogy a gyomorsav termelése a szervezet igényeihez igazodjon.
A protonpumpa működésének pontos megértése elengedhetetlen a gyomor-bélrendszeri betegségek, különösen a savas reflux és a fekélybetegség kezeléséhez. A protonpumpa-gátlók (PPI-k) a gyógyszeres kezelés alapját képezik, hatékonyan csökkentve a gyomorsav termelését a pumpa irreverzibilis gátlásával.
A protonpumpa gátlók (PPI-k) specifikusan a protonpumpához kötődnek, és gátolják annak működését. A PPI-k prodrugok, amelyek a savas környezetben aktiválódnak, így célzottan a parietális sejtekben fejtik ki hatásukat. A PPI-k használata jelentősen javította a savas eredetű betegségek kezelését, de a hosszú távú alkalmazásukkal kapcsolatban is felmerültek kérdések, ezért fontos az orvosi felügyelet.
A gyomorsav termelés szabályozása: hormonális és idegi hatások
A gyomorsav termelését bonyolult hormonális és idegi mechanizmusok szabályozzák, melyek végső soron a protonpumpa (H+/K+ ATPáz) aktivitását befolyásolják a parietális sejtekben. Ez a finomhangolás biztosítja, hogy a gyomor megfelelő mennyiségű savat termeljen az emésztéshez, de ne károsítsa a gyomor falát.
Hormonális szabályozás: A gasztrin, a hisztamin és a szomatosztatin kulcsszerepet játszanak. A gasztrin a gyomor antrumában termelődik, válaszul a gyomor kitágulására, aminosavakra és peptidekre. A gasztrin közvetlenül serkenti a parietális sejteket, valamint közvetetten, az ECL (enterochromaffin-like) sejtek hisztamin termelésének fokozásával. A hisztamin az ECL sejtekből szabadul fel, és a parietális sejteken található H2 receptorokhoz kötődve serkenti a protonpumpa működését, ezáltal növelve a savtermelést.
A szomatosztatin gátló hatású. A D sejtek termelik a gyomorban, és gátolja a gasztrin és a hisztamin felszabadulását, ezáltal csökkentve a savtermelést. A szomatosztatin termelését a gyomorsavasság növekedése serkenti, ami egy negatív visszacsatolási mechanizmust hoz létre.
Idegi szabályozás: A vagus ideg (bolygóideg) mind serkentő, mind gátló hatással bír a gyomorsav termelésére. A vagus ideg acetilkolint szabadít fel, ami közvetlenül serkenti a parietális sejteket (bár kevésbé hatékonyan, mint a gasztrin vagy a hisztamin), valamint serkenti a gasztrin felszabadulását a G sejtekből. Ezen kívül a vagus ideg a GRP (gastrin-releasing peptide) felszabadításával is fokozza a gasztrin termelést.
A vagus ideg által mediált savtermelés két fázisra osztható: a cefálikus fázis (az étel látványa, szaga, íze) és a gasztrikus fázis (az étel a gyomorban). Az intestinalis fázis kevésbé jelentős a gyomorsav termelés szempontjából.
A protonpumpa aktiválása végső soron ezen hormonális és idegi hatások integrált eredménye, melyek együttesen szabályozzák a parietális sejtek intracelluláris jelátviteli útvonalait.
Az intracelluláris jelátviteli útvonalak, mint például a cAMP és a kalcium útvonalak, kulcsfontosságúak a protonpumpa membránba való transzlokációjában és aktiválásában. A hisztamin a cAMP útvonalat aktiválja, míg a gasztrin és az acetilkolin a kalcium útvonalat. Ezek az útvonalak foszforilációs kaszkádokat indítanak el, melyek a protonpumpa működéséhez szükséges enzimek aktiválásához vezetnek.
A gyomorsav termelés szabályozásának megértése elengedhetetlen a gyomorfekély, a reflux betegség és más gyomor-bélrendszeri betegségek kezelésében. A protonpumpa gátlók (PPI-k) hatékonyan csökkentik a savtermelést, mivel közvetlenül gátolják a protonpumpa működését, függetlenül a hormonális és idegi stimulációtól.
Hisztamin, acetilkolin és gasztrin szerepe a gyomorsav szekréció stimulálásában
A gyomorsav termelése egy szigorúan szabályozott folyamat, amelyben a protonpumpa (H+/K+ ATPáz) kulcsszerepet játszik. Ezt a pumpát, amely a parietális sejtek membránjában található, három fő inger stimulálja: a hisztamin, az acetilkolin és a gasztrin. Mindhárom anyag különböző receptorokon keresztül fejti ki hatását, végső soron a protonpumpa aktiválását eredményezve.
A hisztamin a parietális sejteken található H2 receptorokhoz kötődik. Ez a kötődés aktiválja az adenilát-ciklázt, ami növeli a sejten belüli ciklikus AMP (cAMP) szintet. A megnövekedett cAMP serkenti a protein kináz A-t (PKA), ami foszforilálja a protonpumpát és más intracelluláris fehérjéket, elősegítve a pumpa membránhoz kerülését és aktiválását. Így a hisztamin közvetlenül serkenti a savszekréciót.
Az acetilkolin, melyet a vagus ideg szabadít fel, a parietális sejteken található M3 muszkarin receptorokhoz kötődik. Ez a kötődés a foszfolipáz C (PLC) aktiválását idézi elő, ami növeli az intracelluláris kalcium (Ca2+) szintet. A megnövekedett kalcium szint aktiválja a protein kináz C-t (PKC), ami szintén foszforilálja a protonpumpát és más intracelluláris fehérjéket, elősegítve a savszekréciót. Az acetilkolin ezenkívül közvetlenül is serkentheti a hisztamin felszabadulását az ECL sejtekből, ezáltal közvetetten is növelve a savtermelést.
A gasztrin, melyet a G sejtek termelnek a gyomor antrumában, a parietális sejteken található CCK2 receptorokhoz kötődik. Hasonlóan az acetilkolinhoz, a gasztrin is a PLC aktiválásán keresztül növeli az intracelluláris kalcium szintet, ami a PKC aktiválásához és a savszekrécióhoz vezet. Ezen felül a gasztrin serkenti a hisztamin felszabadulását az ECL sejtekből, ami tovább fokozza a savtermelést.
A hisztamin, acetilkolin és gasztrin mindhárman különböző útvonalakon keresztül hatnak, de végső soron a protonpumpa aktiválásához vezetnek, ami a gyomorsav szekréciójának meghatározó eleme.
Fontos megjegyezni, hogy ezek a stimuláló tényezők szinergikusan is hatnak. Például, a hisztamin jelenléte fokozhatja az acetilkolin és a gasztrin hatását, és fordítva. Ez a komplex szabályozási rendszer biztosítja, hogy a gyomorsav termelése a szervezet igényeihez igazodjon.
A szomatosztatin és más gátló tényezők hatása a gyomorsav termelésre
A gyomorsav termelés finomhangolásában számos gátló tényező játszik kulcsszerepet, melyek a parietális sejtek protonpumpájának (H+/K+-ATPáz) működését befolyásolják. Ezek közül a szomatosztatin kiemelkedő jelentőségű.
A szomatosztatin egy peptid hormon, melyet a D-sejtek termelnek a gyomorban és a duodenum falában. A szomatosztatin hatásmechanizmusa komplex. Egyrészt közvetlenül gátolja a parietális sejteket, csökkentve a protonpumpa aktivitását. Másrészt közvetetten is hat, ugyanis gátolja a hisztamin felszabadulását az ECL sejtekből (enterokromaffin-szerű sejtek), ami a gyomorsav termelés egyik fő stimulátora.
További gátló tényezők közé tartoznak a prosztaglandinok. Ezek a lipidmediátorok védő hatást fejtenek ki a gyomor nyálkahártyáján, többek között a gyomorsav szekréció csökkentésével. A nem-szteroid gyulladáscsökkentők (NSAID-ok) gátolják a prosztaglandinok szintézisét, ezáltal növelhetik a gyomorsav termelést és a fekélyek kialakulásának kockázatát.
A gyomorsav termelést gátolhatják továbbá bizonyos gyógyszerek, például a H2-receptor antagonisták, melyek a hisztamin hatását blokkolják a parietális sejteken.
A szomatosztatin tehát egy központi szabályozó, mely a parietális sejtek működésén keresztül, a protonpumpa aktivitásának csökkentésével jelentősen mérsékli a gyomorsav termelést.
Az elégtelen szomatosztatin termelés vagy a gátló tényezők hiánya a gyomorsav túlzott termeléséhez vezethet, ami hozzájárulhat a gyomorfekély és a reflux betegség kialakulásához.
A protonpumpa-gátlók (PPI-k): hatásmechanizmus, típusok és alkalmazási területek
A protonpumpa-gátlók (PPI-k) a gyomorsav-termelés csökkentésének leghatékonyabb eszközei. Működésük a gyomor parietális sejtjeiben található H+/K+-ATPáz enzim (a protonpumpa) irreverzibilis gátlásán alapul. Ez az enzim felelős a hidrogénionok (H+) gyomor lumenébe történő szállításáért, ami a gyomorsav (sósav, HCl) fő komponense. A PPI-k prodrugok, azaz inaktív formában kerülnek be a szervezetbe. A gyomor savas környezetében aktiválódnak, és kovalensen kötődnek a protonpumpához, tartósan inaktiválva azt.
A PPI-k hatásmechanizmusa tehát nem a sav semlegesítésében rejlik, hanem a savtermelés alapvető mechanizmusának megakadályozásában. Ez a hatás tartós, mivel az inaktivált protonpumpákat a szervezetnek újakra kell cserélnie, ami időbe telik. Ezáltal a PPI-k tartósan csökkentik a gyomorsav-termelést.
A PPI-k a leghatékonyabb gyógyszerek a gyomorsav-termelés csökkentésére, mivel közvetlenül a savtermelésért felelős enzimet gátolják.
Számos típusú PPI létezik, amelyek kémiai szerkezetükben és metabolizmusukban különböznek, de hatásmechanizmusuk azonos. A leggyakrabban használt PPI-k közé tartozik az omeprazol, a lansoprazol, a pantoprazol, a rabeprazol és az esomeprazol. A különbségek elsősorban a hatás kezdetének sebességében, a metabolizmus útvonalaiban és a gyógyszerkölcsönhatásokban mutatkoznak meg. Az esomeprazol például az omeprazol S-izomerje, és hatékonyabban gátolja a savtermelést.
A PPI-k alkalmazási területei rendkívül szélesek. Elsősorban a savas reflux betegség (GERD), a gyomorfekély és a nyombélfekély kezelésére használják. Ezenkívül alkalmazzák a Zollinger-Ellison szindróma kezelésére, amely egy ritka betegség, mely túlzott gyomorsav-termeléssel jár. A PPI-k fontos szerepet játszanak a Helicobacter pylori baktérium okozta fertőzések eradikálásában is, melyek gyakran fekélyekhez vezetnek, antibiotikumokkal kombinálva. Végül, a nem-szteroid gyulladáscsökkentő gyógyszerek (NSAID-ok) által okozott gyomorfekélyek megelőzésére is alkalmazzák, különösen azoknál a betegeknél, akiknél magas a fekély kialakulásának kockázata.
A PPI-k mellékhatásai és a hosszú távú használat kockázatai
A protonpumpa-gátlók (PPI-k) hatékonyan csökkentik a gyomorsav termelést, de hosszú távú használatuk számos mellékhatással és kockázattal járhat. Ezek a gyógyszerek befolyásolják a gyomor savasságát, ami kihatással lehet a tápanyagok felszívódására.
Az egyik leggyakoribb probléma a B12-vitamin hiánya, mivel a gyomorsav szükséges a B12-vitamin felszabadításához a táplálékból. A kalcium és a magnézium felszívódása is romolhat, ami csontritkuláshoz és csonttörésekhez vezethet, különösen idősebb betegeknél. Ezenkívül a vashiányos vérszegénység kockázata is nőhet.
A savcsökkentés megváltoztathatja a bélflórát, ami fokozhatja a fertőzések kockázatát. A Clostridium difficile fertőzés, ami súlyos hasmenéssel jár, gyakrabban fordul elő PPI-t szedőknél. Emellett a tüdőgyulladás kockázata is emelkedhet, mivel a gyomorsav hiánya lehetővé teszi a baktériumok bejutását a légutakba.
Ritkább, de súlyosabb mellékhatások közé tartozik a krónikus vesebetegség kialakulásának kockázata, valamint a gyomorpolipok megjelenése. Egyes kutatások összefüggést mutattak a PPI-k és a demencia között is, bár ez a kapcsolat még további vizsgálatokat igényel.
A legfontosabb üzenet az, hogy a PPI-ket csak indokolt esetben és a lehető legrövidebb ideig szabad szedni.
Fontos, hogy a betegek tájékozottak legyenek a lehetséges kockázatokról, és rendszeresen konzultáljanak orvosukkal a PPI-k szedésének szükségességéről és a megfelelő adagolásról. Az orvos felmérheti a kockázatokat és előnyöket, és alternatív kezeléseket javasolhat, ha szükséges.
Alternatív gyomorsav-csökkentő terápiák: H2-receptor antagonisták, antacidák és egyéb módszerek
Bár a protonpumpa-gátlók (PPI-k) rendkívül hatékonyak a gyomorsav termelésének csökkentésében, léteznek alternatív terápiák is, amelyek más mechanizmusokon keresztül fejtik ki hatásukat. Ezek közé tartoznak a H2-receptor antagonisták, az antacidák és bizonyos életmódbeli változtatások.
A H2-receptor antagonisták, mint például a ranitidin vagy a famotidin, a hisztamin H2 receptorait blokkolják a gyomor parietális sejtjein. A hisztamin fontos szerepet játszik a gyomorsav termelésének stimulálásában, így ezek a gyógyszerek csökkentik a savszekréciót, bár kevésbé hatékonyan, mint a PPI-k. Előnyük, hogy gyorsabban hatnak, mint a PPI-k, de hatásuk rövidebb ideig tart.
Az antacidák, mint például a kalcium-karbonát vagy a magnézium-hidroxid, a már megtermelt gyomorsavat semlegesítik. Nem csökkentik a sav termelését, hanem a savas környezetet pufferelik. Gyorsan enyhítik a gyomorégést és a savas reflux tüneteit, de hatásuk rövid ideig tart, és gyakori használatuk mellékhatásokhoz vezethet, például hasmenéshez vagy székrekedéshez.
Bizonyos életmódbeli változtatások is segíthetnek a gyomorsav-termelés szabályozásában. Ezek közé tartozik a dohányzás elhagyása, az alkohol és a koffein fogyasztásának mérséklése, a zsíros és fűszeres ételek kerülése, valamint a kisebb, gyakoribb étkezések. A stresszkezelés és a megfelelő testtartás (például evés után nem azonnal lefeküdni) szintén fontos szerepet játszhatnak a tünetek enyhítésében.
A H2-receptor antagonisták és az antacidák gyors, de rövid távú megoldást nyújtanak a gyomorégés és a savas reflux tüneteire, míg az életmódbeli változtatások hosszú távon segíthetnek a gyomorsav-termelés szabályozásában.
Fontos megjegyezni, hogy ezek az alternatív terápiák nem minden esetben helyettesítik a PPI-k alkalmazását, különösen súlyosabb esetekben. Az orvosával való konzultáció elengedhetetlen a legmegfelelőbb kezelési terv kidolgozásához.
A Helicobacter pylori fertőzés és a gyomorsav termelés kapcsolata
A Helicobacter pylori (H. pylori) fertőzés jelentősen befolyásolja a gyomorsav termelést, ami közvetve a protonpumpa működésére is hatással van. A baktérium által kiváltott gyulladás a gyomor nyálkahártyájában bonyolult folyamatokat indít el.
A fertőzés kezdeti szakaszában a H. pylori gátolja a szomatosztatin termelését. A szomatosztatin egy hormon, amely a gyomorsav termelését csökkenti. Ennek gátlásával a gyomorsav termelése átmenetileg megnőhet, ami a protonpumpák fokozott aktivitását eredményezi. Ez a hiperaciditás azonban nem tartós.
Később, krónikus fertőzés esetén, a H. pylori által kiváltott gyulladás és a gyomor nyálkahártyájának károsodása a gyomorsav termelésének csökkenéséhez vezethet. Ez a folyamat, különösen a gyomor testének (corpus) érintettsége esetén, atrófiás gastritishez vezethet, amelyben a savtermelő sejtek (parietális sejtek) száma csökken.
A H. pylori fertőzés tehát nem csak a gyomorsav termelésének átmeneti növekedését okozhatja, hanem a krónikus gyulladás következtében annak tartós csökkenéséhez is vezethet, ami a protonpumpák aktivitásának csökkenésével jár.
A protonpumpa gátlók (PPI) alkalmazása H. pylori fertőzés esetén komplex kérdés. Egyrészt, a PPI-k csökkentik a gyomorsavat, ami kedvezőtlen környezetet teremt a baktérium számára, és segíthet a H. pylori eradikációs terápiában. Másrészt, a tartós PPI használat növelheti a gyomor pH-ját, ami elősegítheti a H. pylori szaporodását és a gyomor felső részébe való migrációját.
Éppen ezért a H. pylori fertőzés kezelése során a PPI-ket általában antibiotikumokkal kombinálják az eradikáció hatékonyságának növelése érdekében. A kezelés célja a baktérium eltávolítása és a gyomor nyálkahártyájának gyógyulásának elősegítése.