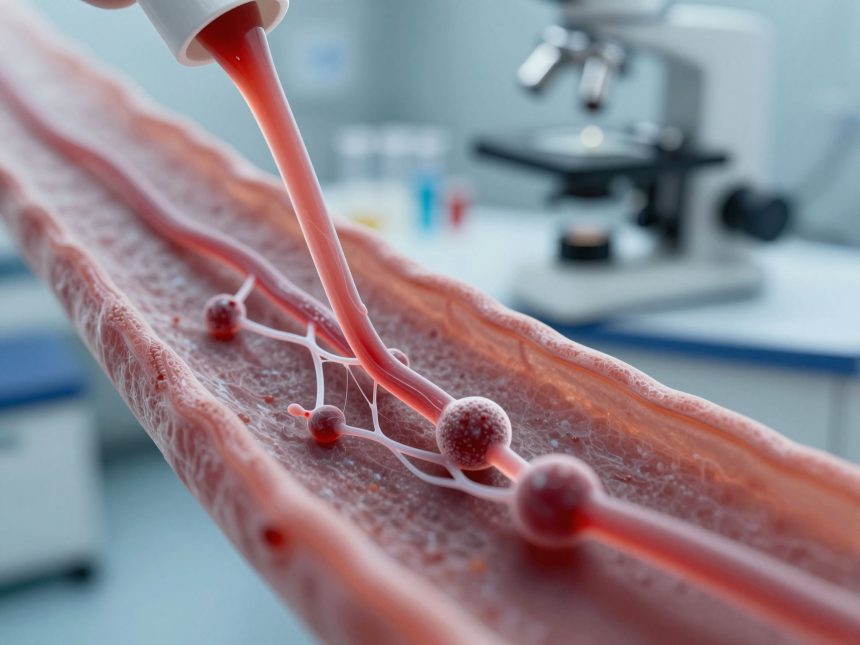
A fibrinogén, más néven Factor I, egy kulcsfontosságú plazmafehérje, amely elengedhetetlen a véralvadási folyamatban és a hemosztázis fenntartásában. Ez a nagy méretű, kettős Y-alakú molekula a májban szintetizálódik, és normál körülmények között a vérplazma egyik legmagasabb koncentrációjú fehérjéje. A hemosztázis, vagyis a vérzés megállítása, egy rendkívül összetett, lépcsőzetes folyamat, amelyben a fibrinogénnek a végső, stabil véralvadék kialakításában van kiemelkedő szerepe.
A véralvadási kaszkád aktiválódása során, különösen az intrinszik és extrinszik út egyaránt a közös útvonalon keresztül a trombin termelődéséhez vezet. A trombin, mint a véralvadási rendszer egyik legfontosabb effektor enzime, számos szubsztrátot képes aktiválni, de legjelentősebb hatása a fibrinogénre gyakorolt átalakító képessége. A trombin eltávolítja a fibrinogén molekula két fibrinopeptid A-ját, ami egy oldható, instabil fibrin monomerré alakítja át.
A fibrinogén átalakulása fibrin monomerré a trombin által a véralvadási folyamat egyik legkritikusabb lépése, amely lehetővé teszi az oldható fehérje oldhatatlan, hálószerű szerkezetté való átalakulását.
Az így keletkezett fibrin monomerek spontán polimerizálódnak, egymáshoz kapcsolódva egy oldhatatlan fibrinpolimer hálózatot alkotnak. Ez a hálózat a mechanikai stabilitást biztosítja a vérrög számára, csapdába ejtve a vérsejteket és a plazmát, ezáltal hatékonyan elzárva a sérült érszakaszt. A fibrin polimerizációja nem csupán fizikai kötődéseken alapul; a folyamatot további fehérjék, mint például a Factor XIII (fibrinstabilizáló faktor) által katalizált kovalens kötések is erősítik, amelyek még ellenállóbbá teszik a kialakuló véralvadékot a fibrinolízissel szemben.
A fibrinogén nem csak a véralvadék mechanikai integritásának biztosításában játszik szerepet. Jelentős hatása van a vérlemezkék aggregációjára is, különösen nagy sebességű áramlás esetén, ahol a fibrinogén hidat képez a vérlemezkék felszínén található glikoprotein receptorok között, elősegítve azok összetapadását. Ezen kívül a fibrinogén modulálja a gyulladásos válaszokat és részt vesz az érfal gyógyulási folyamataiban is, ami tovább hangsúlyozza a hemosztatikus rendszert alkotó komplex kölcsönhatásokat.
A fibrinogén szintjének és funkciójának értékelése létfontosságú a véralvadási zavarok diagnosztizálásában. Alacsony fibrinogénszint (hipofibrinogenémia) vagy a fibrinogén funkciójának zavara (diszfibrinogenémia) jelentős vérzési hajlamhoz vezethet. Ezzel szemben a kórosan emelkedett fibrinogénszint (hiper-fibrinogenémia) fokozott trombózishajlamra utalhat.
A véralvadási kaskád: Az alapoktól a komplexitásig
A véralvadási kaskád két fő útvonalon, az intrinszik és extrinszik úton keresztül aktiválódik, amelyek végül a közös útvonalban futnak össze. Mindkét út célja a trombin, a véralvadási folyamat központi szereplőjének nagy mennyiségű termelése. A fibrinogén ebben a komplex sorozatban az utolsó, de legfontosabb effektor szerepet tölti be, miután a trombin már jelentős mennyiségben jelen van.
Az intrinszik út a vér sérülésekor keletkező negatív töltésű felszínek, például a kollagén vagy az aktivált vérlemezkék hatására indul be. A Factor XII (Hageman faktor) aktiválódása indítja el a folyamatot, ami a Factor XI, majd a Factor IX és X aktiválását eredményezi. Ezzel szemben az extrinszik út a sérült érfal által kibocsátott szöveti faktor (tissue factor, TF) révén aktiválódik, amely közvetlenül a Factor VII-vel képez komplexet, ezáltal aktiválva a Factor X-et.
A Factor Xa, mindkét útvonal közös pontján, a protrombináz komplex részeként (Factor Va és kalciumionok jelenlétében) katalizálja a protrombin (Factor II) átalakulását trombin (Factor IIa) molekulává. A trombin így létrejövő magas koncentrációja elengedhetetlen a fibrinogén hatékony átalakításához.
A trombin nem csupán a fibrinogén oldhatatlan fibrinné alakításáért felelős, hanem pozitív visszacsatolási mechanizmusokon keresztül maga is fokozza saját termelődését, valamint aktiválja a vérlemezkéket és a Factor XIII-at, így biztosítva a véralvadék gyors és hatékony kialakulását.
A trombin által kibocsátott fibrinopeptid A és B molekulák eltávolítása a fibrinogénből nem az egyetlen módja annak, hogy a fibrinogén befolyásolja a véralvadást. A fibrinogén közvetlenül kölcsönhatásba lép a vérlemezkékkel, különösen az αIIbβ3 integrin receptorokon keresztül. Ez a kötődés elengedhetetlen a vérlemezkék aggregációjához, ami a primer hemosztatikus dugó kialakulásának alapja.
A hemosztatikus folyamatok labordiagnosztikájában a fibrinogén szintjének mérése alapvető fontosságú. A protrombin idő (PT) és az aktivált parciális tromboplasztin idő (aPTT) vizsgálatok indirekt módon mutatják a fibrinogén mennyiségét és funkcióját, mivel ezek a tesztek a véralvadási kaszkád különböző szakaszainak működését értékelik. Azonban a specifikus fibrinogén tesztek, amelyek közvetlenül mérik a fibrinogén koncentrációját vagy funkcióját, sokkal pontosabb képet adnak.
A hipofibrinogenémia, vagyis az alacsony fibrinogénszint, lehet veleszületett vagy szerzett. A veleszületett formák ritkák, és gyakran súlyos vérzési rendellenességekkel járnak. A szerzett hipofibrinogenémia oka lehet például a májbetegség (mivel a máj termeli a fibrinogént), DIC (disszeminált intravaszkuláris koagulopátia), vagy súlyos vérvesztés.
A diszfibrinogenémia, ahol a fibrinogén molekula szerkezete vagy funkciója kóros, szintén vérzési hajlamot okozhat. Ezek a betegek gyakran rendelkeznek normál fibrinogén koncentrációval, de a molekula nem képes megfelelően polimerizálódni vagy keresztes kötődni. Ezzel szemben, a hiperfibrinogenémia, azaz a magas fibrinogénszint, nem feltétlenül jelent kóros állapotot, de gyakran társul gyulladásos folyamatokkal vagy kardiovaszkuláris kockázati tényezőkkel, és növelheti a trombózis hajlamot.
A fibrinogén szerkezete és funkciója a véralvadási kaskádban
A fibrinogén egy komplex, dimetrikus fehérje, amely három különböző polipeptid láncból áll: Aα, Bβ és γ. Ezek a láncok diszulfid kötésekkel kapcsolódnak össze, egy jellegzetes, kettős Y-alakú molekulát alkotva. A molekula két végén található E-doménok és a középső részen elhelyezkedő D-doménok kulcsfontosságúak a polimerizációs folyamatban. A fibrinogénnek a véralvadási kaskádban betöltött szerepe szorosan összefügg ezen szerkezeti elemek funkciójával.
Amikor a trombin (Factor IIa) aktiválódik a véralvadási kaszkádban, specifikusan hasítja el a fibrinogén Aα és Bβ láncaihoz kapcsolódó fibrinopeptid A és B molekulákat. Ez a proteolitikus hasítás teszi lehetővé a fibrinogén molekula konformációjának megváltozását, ami exponálja a D-doménok és az E-doménok közötti kötőhelyeket. Ezek a helyek kritikusak a fibrin monomer egységek egymáshoz való kapcsolódásában, ami a fibrinpolimer hálózat kialakulásának alapja.
A trombin által katalizált fibrinopeptid eltávolítás a fibrinogénből egy irreverzibilis lépés, amely elengedhetetlen a fibrinmonomerek spontán polimerizációjához és az oldhatatlan véralvadék fizikai stabilitásának megteremtéséhez.
Az így keletkezett fibrin monomerek, miután felszabadultak a fibrinopeptidek alól, spontán rendeződnek és polimerizálódnak. A fibrinmonomerek hosszanti irányban kapcsolódnak egymáshoz, az E-doménok a D-doménokhoz kötődnek, míg az oldalirányú kapcsolódások is létrejönnek a D-doménok között. Ez a rendezett polimerizáció hozza létre a jellegzetes fibrilláris szerkezetet, amely a véralvadék gerincét adja. A fibrin hálózat pórusmérete változó, és befolyásolja a benne csapdába eső vérsejtek és plazma áramlását.
A fibrin polimerizációját tovább erősíti a Factor XIII (FXIII), a fibrinstabilizáló faktor. A trombin és a kalciumionok aktiválják az FXIII-at, amely ezután kovalens kötéseket hoz létre a fibrin polimerek D-doménjai között. Ez a keresztes kötődés nagymértékben növeli a véralvadék mechanikai szilárdságát és ellenállását a fibrinolitikus enzimekkel, például a plazminnal szemben, biztosítva a véralvadék integritását a sebgyógyulás során.
A fibrinogén nem csak a fibrin hálózat építőköve. A vérlemezkék felszínén található GP IIb/IIIa (αIIbβ3) integrin receptorokhoz való kötődése révén kulcsszerepet játszik a vérlemezkék aggregációjában, különösen a nagy nyíróerővel bíró áramlási viszonyok között. Ez a hidat képező funkció biztosítja a primer hemosztatikus dugó kialakulását a sérült érfelszínen, mielőtt a fibrinpolimer hálózat stabilizálná azt.
A fibrinogén szerkezetének vagy mennyiségének zavarai, mint a hipofibrinogenémia és a diszfibrinogenémia, közvetlenül befolyásolják a véralvadék kialakulásának képességét és stabilitását. A hipofibrinogenémiában szenvedő betegeknél a véralvadék nem tud megfelelően kialakulni az alacsony fibrinogénszint miatt, míg a diszfibrinogenémiában a fibrinogén molekulák funkcionális hibái gátolják a polimerizációt vagy a stabilizációt, hasonlóan súlyos vérzési rendellenességeket okozva.
A fibrinogén aktiválása: Trombin szerepe és a fibrin polimerizációja
A fibrinogén aktiválásának kulcsfontosságú lépése a trombin által végzett specifikus proteolitikus hasítás. A trombin, a véralvadási kaszkád központi enzime, a fibrinogén molekula két különböző helyen fejti ki hatását: eltávolítja az N-terminális fibrinopeptid A-t (FpA) és a C-terminális fibrinopeptid B-t (FpB). Ez a kettős hasítás alapvető a fibrin monomerek képződéséhez, amelyek aztán képesek polimerizálódni.
A FpA eltávolítása elsődlegesen történik, és ez az, ami a fibrin monomert képessé teszi az önálló polimerizációra. A FpB eltávolítása, bár ez is hozzájárul a polimer szerkezetéhez, kevésbé kritikus a kezdeti aggregációhoz. Az így létrejött fibrin monomerek képesek egymáshoz kapcsolódni, hosszú, párhuzamos szálakat képezve. Ez a folyamat nem véletlenszerű; a fibrinogén molekulák specifikus kötőhelyek révén találják meg egymást. Az FpA eltávolítása után felszabadul egy új kötőhely a fibrin monomeren, amely képes kapcsolódni egy másik fibrin monomeren lévő, korábban a FpB által fedett régióhoz.
A trombin által a fibrinogénből eltávolított fibrinopeptidek nem csak a polimerizációt teszik lehetővé, hanem szabályozó szerepet is betöltenek a véralvadásban, befolyásolva a trombin aktivitását és a vérlemezkék működését.
Az egymásra épülő fibrin szálak egy térhálós szerkezetet alkotnak, amely magába zárja a vérlemezkéket, a vörösvértesteket és a plazmát. Ez a mechanikai hálózat az, ami a vérrög szilárdságát és stabilitását biztosítja. A kezdeti fibrin polimer nem rendelkezik nagy mechanikai ellenállással, de a Factor XIIIa (fibrinstabilizáló faktor), amelyet szintén a trombin aktivál, kovalens keresztes kötéseket hoz létre a fibrin szálak között. Ezek a keresztes kötések drámaian megnövelik a kialakuló véralvadék ellenállását a mechanikai és fibrinolitikus hatásokkal szemben.
A fibrin polimerizációjának sebessége és hatékonysága számos tényezőtől függ. Ide tartozik a trombin koncentrációja, a fibrinogén koncentrációja, valamint a vérplazmában található egyéb fehérjék jelenléte, amelyek befolyásolhatják a polimerizációs folyamatot. A normálisan működő vérlemezkék is jelentős szerepet játszanak a fibrin hálózat kialakulásában, mivel felületükön a fibrinogén hidakat képezve segítik a fibrin szálak rendeződését és rögzülését.
A labordiagnosztikában a fibrinogén aktivációjának és a fibrin polimerizációjának megértése kulcsfontosságú. A trombin idő (TT) teszt közvetlenül méri a vérplazma fibrint szilárdá alakító képességét. Ebben a tesztben ismert mennyiségű trombin kerül hozzáadásra a beteg plazmájához, és mérik, mennyi idő alatt alakul ki a fibrinrög. A megnyúlt trombin idő utalhat alacsony fibrinogén szintre, dysfibrinogenémiára, vagy heparin jelenlétére a mintában.
A fibrinogén funkcionális tesztek, amelyek az FpA és FpB eltávolítását és az ezt követő polimerizációt vizsgálják, tovább árnyalják a képet. Ezek a tesztek segítenek megkülönböztetni a mennyiségi problémákat (alacsony fibrinogén szint) a minőségi problémáktól (diszfibrinogenémia), ahol a molekula szerkezete vagy funkciója sérült. A diszfibrinogenémiák gyakran öröklött rendellenességek, amelyek közül néhány klinikai tünetek nélkül is jelen lehet, míg mások súlyos vérzési hajlamot okoznak a fibrin polimerizációjának elégtelensége miatt.
Hemosztatikus folyamatok: A véralvadás szerepe a sebgyógyulásban és a vérzés megállításában
A véralvadék, melynek stabilizálásában a fibrin kulcsszerepet játszik, nem csupán a vérzés megállítására szolgál, hanem alapvető fontosságú a sebgyógyulási folyamatok elindításában és támogatásában is. A frissen kialakult fibrin hálózat nem csak mechanikai gátat képez, hanem egyfajta matricaként is funkcionál, amelyhez különböző sejtek, mint például a fibroblasztok és az endotél sejtek kötődhetnek. Ez a sejtes „kötődés” elengedhetetlen az új szövetek kialakulásához és az érszövet regenerációjához.
A véralvadékban csapdába esett növekedési faktorok, citokinek és más bioaktív molekulák fokozatosan szabadulnak fel, stimulálva a sejtek proliferációját és migrációját a sérült területre. A fibrinogén és a belőle keletkező fibrin közvetlen szerepet játszik ezen faktorok tárolásában és felszabadításában, így befolyásolva a seb gyógyulásának sebességét és minőségét. A fibrinogén hiánya vagy diszfunkciója így nem csak vérzékenységet, hanem késleltetett sebgyógyulást is eredményezhet.
A fibrinogén nem pusztán a vérzés megállításának eszköze, hanem aktívan részt vesz a sejtes kommunikációban és a regenerációs folyamatokban a sérült szövetekben.
A hemosztatikus folyamatok labordiagnosztikájában a fibrinogén funkcionális vizsgálatai különösen fontosak lehetnek. Míg a fibrinogén koncentrációjának mérése megadja a molekula mennyiségét, addig a funkcionális tesztek (például a trombin idő, amely a fibrinogén trombin általi átalakulásának sebességét méri) arra is fényt deríthetnek, hogy a molekula képes-e megfelelően betölteni funkcióját. A diszfibrinogenémia esetében a koncentráció normális lehet, de a funkció károsodott, ami speciális vizsgálatokat tesz szükségessé.
A DIC (disszeminált intravaszkuláris koagulopátia) egy életveszélyes állapot, ahol a véralvadási rendszer generalizált aktivációja következik be. Ebben a szindrómában a fibrinogén fokozottan felhasználódik a kiterjedt mikrovérrögképződés során, ami hipofibrinogenémiához vezet. A fibrinogén szintjének csökkenése a DIC egyik jellegzetes laboratóriumi lelete, és súlyos vérzési kockázatot jelez. Ezzel szemben a gyulladásos folyamatok, fertőzések vagy bizonyos daganatos megbetegedések akut fázis reakció részeként emelhetik a fibrinogén szintjét. Ez a jelenség, a hiper-fibrinogenémia, nem mindig kóros, de összefüggésbe hozható a gyulladással és a kardiovaszkuláris betegségek fokozott kockázatával.
A fibrinogén molekula modulálja a gyulladásos válaszokat, befolyásolva a leukociták adhézióját és migrációját a gyulladás helyszínére. Ezáltal a fibrinogén nem csupán a véralvadásban, hanem az immunrendszer működésében is szerepet játszik, ami tovább növeli komplexitását a hemosztatikus és gyulladásos folyamatokban.
A fibrinogén laboratóriumi meghatározásának módszerei
A fibrinogén laboratóriumi meghatározására többféle módszer áll rendelkezésre, amelyek eltérő elven működnek, és különböző információkat nyújtanak a fibrinogén mennyiségéről és funkciójáról. A leggyakrabban használt eljárások a kromogén tesztek és a turbidimetriás módszerek.
A kromogén tesztek alapvetően a fibrinogén mennyiségének funkcionális meghatározására szolgálnak. Ezek a módszerek kihasználják, hogy a trombin képes a fibrinogénből fibrint képezni. A teszt során a mintában lévő fibrinogént nagy koncentrációjú trombinnal inkubálják, ami fibrin képződéséhez vezet. Ezt követően egy specifikus, kromogén szubsztrátot adnak hozzá, amely a trombin által az inkubáció során keletkező aktív enzimekkel reagálva színes terméket hoz létre. A keletkezett szín intenzitása közvetlenül arányos a véralvadási mintában lévő aktív trombin mennyiségével, ami viszont a kiinduló fibrinogén mennyiségétől függ. Ez a módszer pontosan méri az oldható, funkcionális fibrinogén mennyiségét.
A turbidimetriás módszerek, beleértve a turbidimetriás és nephelometriás eljárásokat, a fibrinogén koncentrációjának kvantitatív meghatározására alkalmasak. Ezek a módszerek a fibrinogén molekulák által okozott fényelnyelés vagy fényszóródás mérésén alapulnak. A minta plazmájához specifikus reagenst adnak, amely a fibrinogénnel kicsapódó komplexet képez. A keletkezett zavarosság mértéke, vagyis a fény elnyelődése vagy szóródása, közvetlenül korrelál a fibrinogén koncentrációjával a mintában. Ezek a módszerek gyorsak és automatizálhatók, így széles körben alkalmazzák őket a rutin laboratóriumi gyakorlatban.
A laboratóriumi vizsgálatok során a fibrinogén szintjének meghatározása kulcsfontosságú a véralvadási zavarok diagnosztizálásában, mivel a normálértékektől való eltérések jelentős klinikai következményekkel járhatnak.
Fontos megemlíteni a clauss-módszert, amely szintén a funkcionális fibrinogén mérésére szolgál. Ez a módszer egy speciális, fibrinogén-hiányos plazmát használ standardként, amelyhez a vizsgálandó plazmát adják. A keverékhez trombin és kalciumionok hozzáadásával a fibrinogén polimerizációja és a véralvadék kialakulása indul be. A véralvadék kialakulásához szükséges idő mérése alapján határozható meg a vizsgálandó plazma fibrinogén koncentrációja. Rövidebb alvadási idő magasabb fibrinogénszintre utal.
Ezen kívül léteznek immunológiai módszerek is, mint például az ELISA (enzim-linked immunosorbent assay), amelyek a fibrinogén specifikus antitestekkel való reakcióján alapulnak. Ezek a módszerek képesek mérni az összes fibrinogént, beleértve a funkcionálisan inaktív formákat is, így eltérő információt nyújthatnak a funkcionális tesztekhez képest.
A különböző módszerek közötti választás függ a laboratórium kapacitásától, a rendelkezésre álló automatizáltságtól, valamint a klinikai kérdéstől. Például, ha funkcionális zavarra gyanakszunk, a kromogén vagy Clauss-módszer előnyösebb lehet, míg a mennyiségi meghatározáshoz a turbidimetriás eljárások is elegendőek lehetnek.
Fibrinogén meghatározás: Klinikai jelentőség és értelmezés
A fibrinogén meghatározása a laboratóriumi diagnosztika egyik alapvető vizsgálata a véralvadási rendellenességek felderítésében. Különböző módszerek állnak rendelkezésre a fibrinogén mennyiségi és funkcionális vizsgálatára, amelyek mindegyike más-más klinikai információt szolgáltat. A legegyszerűbb, bár indirekt módszer a rutinszerű véralvadási tesztek (PT, aPTT) eredményeinek értékelése, amelyek megnyúlása utalhat fibrinogén hiányra vagy funkciózavarra.
A közvetlen fibrinogén mérések pontosabb képet adnak. A turbidimetriás vagy nefelometriás módszerek a plazmában lévő fibrinogén mennyiségét határozzák meg, míg a kromogén tesztek a fibrinogén aktiválási potenciálját vagy a trombin hatására történő átalakulás sebességét mérik. A funkcionális fibrinogén tesztek, mint például a Clauss-módszer, a trombin által katalizált polimerizáció sebességét értékelik, ami közvetlenül tükrözi a fibrinogén azon képességét, hogy stabil véralvadékot képezzen.
A klinikai jelentőség a fibrinogénszint és funkció eltéréseinek megértésében rejlik, mivel ezek az eltérések közvetlenül befolyásolják a vérzés vagy a trombózis kockázatát.
Az alacsony fibrinogénszint (hipofibrinogenémia) esetén a vérzés kockázata megnő. A veleszületett hipofibrinogenémia, mint az afibrinogenémia (teljes fibrinogénhiány) vagy a hipofibrinogenémia, súlyos vérzési hajlamot okoz, amely már újszülött korban vagy korai gyermekkorban jelentkezhet. A szerzett hipofibrinogenémia gyakran súlyosabb betegségek, például májbetegség, disszeminált intravaszkuláris koagulopátia (DIC), vagy jelentős vérvesztés következménye lehet.
A diszfibrinogenémia, ahol a fibrinogén molekula szerkezete kóros, a véralvadék képződésének hatékonyságát csökkenti. Ilyenkor a fibrinogén koncentrációja normális lehet, de a molekula nem képes megfelelően polimerizálódni vagy a Factor XIII által stabilizálódni, ami szintén vérzési rendellenességekhez vezethet. Érdekesség, hogy diszfibrinogenémiában szenvedő betegeknél néha trombózis is előfordulhat, ami a molekuláris defektus komplex hatásaira utal.
A magas fibrinogénszint (hiperfibrinogenémia) önmagában nem feltétlenül patológiás, de gyakran gyulladásos folyamatok, fertőzések, daganatos megbetegedések, vagy kardiovaszkuláris betegségek markerjeként szolgál. A krónikusan emelkedett fibrinogénszint növelheti a trombózis kockázatát, mivel a több fibrinogén több lehetőséget teremt a stabil véralvadék képződésére, és gátolhatja a fibrinolízist. Az értelmezés során mindig figyelembe kell venni a páciens klinikai állapotát és a többi laboratóriumi eredményt.
A laboratóriumi eredmények értelmezése során figyelembe kell venni a minta vételi körülményeit is. Például a nem megfelelő antikoaguláns használata vagy a minta lassú feldolgozása fals eredményekhez vezethet. A különböző mérési módszerek eltérő érzékenységgel bírhatnak, ezért fontos tudni, hogy melyik módszerrel történt a mérés, különösen a ritka fibrinogén defektusok gyanúja esetén.
Fibrinogén rendellenességek: Okok, tünetek és kezelési lehetőségek
A fibrinogén szintjének csökkenése (hipofibrinogenémia) vagy funkciójának zavara (diszfibrinogenémia) komoly következményekkel járhat a véralvadási képességre. Ezek a rendellenességek veleszületettek vagy szerzettek lehetnek, és mindkét esetben jelentős vérzési hajlamot okozhatnak.
A veleszületett hipofibrinogenémia ritka genetikai betegség, amely a fibrinogén termelésének részleges vagy teljes hiányát jelenti. Az afibrinogenémia, a fibrinogén teljes hiánya, a legritkább és legszélsőségesebb forma, amely súlyos, életveszélyes vérzésekkel járhat már születéskor vagy kisgyermekkorban. A hipofibrinogenémia enyhébb formái, ahol a fibrinogén mennyisége csökkent, de nem hiányzik teljesen, kevésbé súlyos, de még mindig jelentős vérzékenységet okozhatnak, különösen traumák vagy műtétek során.
A szerzett hipofibrinogenémia hátterében számos ok állhat. A májbetegségek, mint például a cirrhosis, jelentősen csökkenthetik a fibrinogén szintézisét, mivel a máj felelős a fibrinogén előállításáért. A disszeminált intravaszkuláris koagulopátia (DIC), egy súlyos, életveszélyes állapot, amelyben a véralvadási rendszer kiterjedten aktiválódik, nagymértékű fibrinogén fogyasztást eredményezhet. Súlyos vérvesztés esetén is előfordulhat a fibrinogén szintjének csökkenése, mivel a szervezet nem képes elegendő mennyiségben pótolni. Bizonyos gyógyszerek, például bizonyos antikoagulánsok, is befolyásolhatják a fibrinogén szintjét.
A diszfibrinogenémia esetén a fibrinogén molekula mennyisége normális lehet, azonban annak szerkezete vagy funkciója kóros. Ez azt jelenti, hogy a fibrinogén nem képes megfelelően átalakulni stabil fibrinné, vagy nem képes hatékonyan részt venni a véralvadék stabilizálásában. Ennek oka lehet az aminosav-szekvencia eltérése a fibrinogén molekulában, ami befolyásolja annak trombinnal való kölcsönhatását vagy a polimerizáció képességét. A diszfibrinogenémia tünetei változóak lehetnek, az enyhe vérzékenységtől a súlyosabb vérzési epizódokig.
A fibrinogén rendellenességek tünetei nagymértékben függnek a rendellenesség súlyosságától és típusától, de leggyakrabban vérzékenység formájában jelentkeznek, mint például az orrvérzés, ínyvérzés, véraláfutások, vagy hosszabb ideig tartó vérzés sérülések után.
A kezelési lehetőségek a fibrinogén rendellenesség okától és súlyosságától függenek. Enyhébb esetekben, ahol a vérzés kockázata alacsony, nincs szükség specifikus kezelésre. Súlyosabb vérzési hajlam esetén a fibrinogén koncentrátumok adása a leggyakoribb kezelési módszer. Ezek a készítmények közvetlenül pótolják a hiányzó vagy funkcióját vesztett fibrinogént, gyorsan helyreállítva a véralvadási képességet. DIC esetén a per underlying ok kezelése elsődleges, de a fibrinogén pótlás is szükségessé válhat.
A laboratóriumi vizsgálatok kulcsfontosságúak a fibrinogén rendellenességek diagnosztizálásában. A fibrinogén mennyiségi meghatározása (turbidimetriás vagy kromogén módszerekkel) és a funkcionális tesztek (például a trombin idő, amely a fibrinogén trombin általi átalakulását méri) segítenek megkülönböztetni a hipofibrinogenémiát a diszfibrinogenémiától.
A fibrinogén szintjének emelkedése (hiperfibrinogenémia), amelyről a korábbi szakaszok is említést tettek, nem feltétlenül kóros, gyakran gyulladásos folyamatok vagy terhesség kísérőjelensége. Azonban növelheti a trombózishajlamot, és ezért bizonyos esetekben további kivizsgálást igényelhet.
A fibrinogén szerepe nem-hemosztatikus folyamatokban
Bár a fibrinogén elsődleges szerepe a véralvadásban rejlik, kutatások kimutatták nem-hemosztatikus funkcióit is, amelyek túlmutatnak a vérrög képzésén. Ezek a funkciók különösen fontosak az immunrendszer szabályozásában és az endoteliális sejtek működésében.
A fibrinogén képes kölcsönhatásba lépni különböző immunsejtekkel, mint például a neutrofilokkal és a makrofágokkal. Ezek az interakciók befolyásolhatják az immunsejtek adhézióját és migrációját a gyulladásos területekre, így közvetve részt vesz a gyulladásos válaszok modulálásában. Ez a képesség magyarázatot adhat arra, miért emelkedik gyakran a fibrinogénszint gyulladásos állapotok során, mint egy akut fázis fehérje.
A fibrinogén nem csupán a véralvadék mechanikai stabilitását biztosítja, hanem aktívan részt vesz az immunválaszok és a gyulladásos folyamatok szabályozásában is.
Ezen kívül a fibrinogén szerepet játszik az endoteliális sejtek proliferációjában és migrációjában, ami kulcsfontosságú az érfal integritásának fenntartásában és a sebgyógyulásban. Az érfal sérülésekor a fibrinogén nem csak a véralvadék képződésében segít, hanem elősegítheti az érfal sejtek regenerációját is. Azonban túlzott jelenléte vagy kóros aktivitása hozzájárulhat az atheroszklerózis kialakulásához, ami ismét a hemosztatikus és nem-hemosztatikus funkciók közötti finom egyensúlyra hívja fel a figyelmet.
A véralvadási tesztek (mint a PT és az aPTT) mellett, a funkcionális fibrinogén tesztek különösen fontosak a diszfibrinogenémiák kimutatásában, ahol a molekula mennyisége normális, de működése károsodott. Ezek a tesztek segítenek megkülönböztetni a valódi fibrinogénhiányt a funkcionális problémáktól, ami elengedhetetlen a megfelelő terápiás megközelítés kiválasztásához.