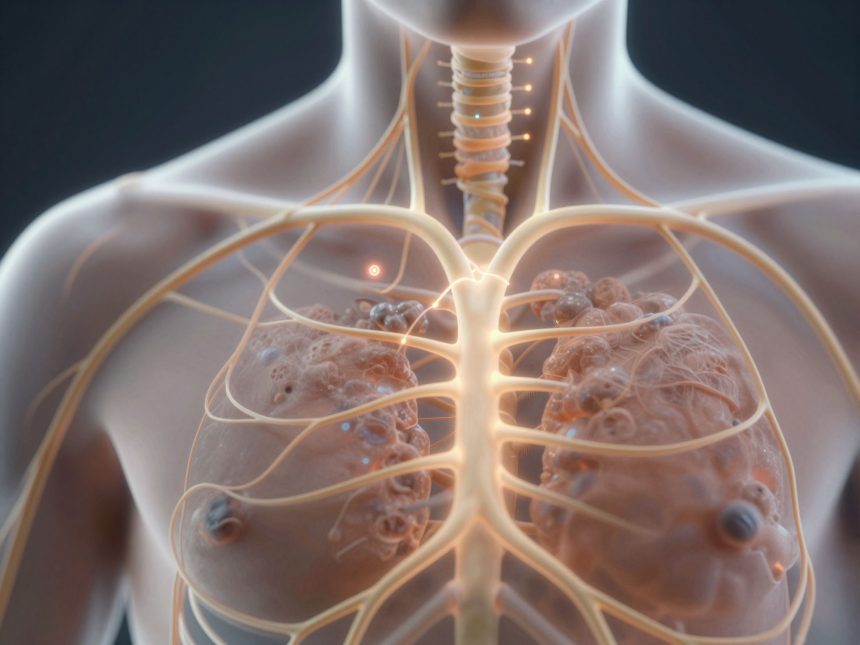
Az emberi szervezet egy rendkívül összetett önszabályozó rendszerrel rendelkezik, amelynek egyik kulcsfontosságú eleme a vegetatív idegrendszer. Ez a rendszer felelős számos létfontosságú, akaratunktól független folyamat szabályozásáért, mint például a szívverés, a légzés, az emésztés és a testhőmérséklet. A vegetatív idegrendszer két fő részből áll: a szimpatikus és a parasimpatikus idegrendszerből. Bár egymással ellentétes hatásokat fejtenek ki, harmonikus együttműködésük biztosítja a belső egyensúly, azaz a homeosztázis fenntartását.
A stresszhelyzetekben a szimpatikus idegrendszer válik dominánssá. Ez a rész felelős az úgynevezett „harcolj vagy menekülj” (fight-or-flight) válasz aktiválásáért. Amikor a szervezet veszélyt észlel, legyen az fizikai fenyegetés vagy pszichés nyomás, a szimpatikus idegrendszer azonnali, drasztikus változásokat indít el a test működésében, hogy felkészítse azt a lehetséges küzdelemre vagy elkerülésre.
A szimpatikus idegrendszer aktiválódása egy komplex, koordinált válaszreakció, amelynek célja a túlélés biztosítása a fenyegető helyzetekben.
Ennek a válasznak a részeként számos fiziológiai változás megy végbe. Megfigyelhető például a szívverés felgyorsulása és a vérnyomás emelkedése, amelyek biztosítják, hogy több oxigénben gazdag vér jusson az izmokhoz és az agyhoz. A légzés sekélyebbé és gyorsabbá válik, hogy növelje a szervezet oxigénfelvételét. A pupillák kitágulnak, hogy javítsák a látást és a környezet jobb észlelését. Ezenkívül a gyomor- és bélmozgások lelassulnak, mivel az emésztés ebben a kritikus helyzetben nem elsődleges fontosságú.
A szimpatikus idegrendszer hatásai nem csak közvetlen idegi impulzusokon keresztül érvényesülnek. Az idegvégződésekből felszabaduló neurotranszmitterek, mint például a noradrenalin, hormonális hatást is kifejthetnek. A mellékvesevelő által termelt adrenalin (epinefrin) és noradrenalin (norepinefrin) szintén jelentős szerepet játszik a stresszválaszban, tovább fokozva a fent említett élettani változásokat. Ezek a hormonok a véráramba kerülve az egész testre kiterjedő hatást fejtenek ki, felkészítve a szervezetet a gyors és hatékony cselekvésre.
Ez a primitív, de rendkívül hatékony adaptációs mechanizmus évmilliókon keresztül segítette az emberi faj fennmaradását. A modern életben azonban a stresszorok gyakran krónikusak, és a szimpatikus idegrendszer tartós aktiválódása negatív hatással lehet az egészségre, hozzájárulva különböző betegségek kialakulásához.
A szimpatikus idegrendszer anatómiája és élettana
A szimpatikus idegrendszer az autonóm idegrendszer egyik fő ága, amelynek kiterjedt hálózata szinte az egész testet behálózza. Ezen idegpályák központi irányítása a gerincvelőből ered, egészen pontosan a thorakális (mellkasi) és lumbális (ágyéki) szegmentumokból. Az innen kiinduló preganglionáris neuronok rövid axonokkal rendelkeznek, amelyek a szimpatikus törzs ganglionjaihoz futnak. Ezek a ganglionok párosan helyezkednek el a gerincvelő mindkét oldalán, egyfajta „láncot” alkotva, amelyet truncus sympathicusnak nevezünk. Itt történik az első szinaptikus átkapcsolás, ahol a preganglionáris neuronok neurotranszmitterként acetilkolint használnak, és a posztganglionáris neuronok szinapszisba lépnek.
A posztganglionáris neuronok axonjai már hosszabbak, és továbbterjednek a cél szervekhez. Ezek a szervek lehetnek belsőségek, erek, mirigyek vagy akár hajszálerek is. A posztganglionáris szimpatikus neuronok elsődleges neurotranszmittere a noradrenalin, amely a legtöbb célsejten alfa- és béta-adrenerg receptorokhoz kötődve fejti ki hatását. Ezek a receptorok eltérő élettani válaszokat váltanak ki. Például az erek simaizomzatában található alfa-receptorok összehúzódást, míg a szívben található béta-receptorok gyorsulást és erősebb összehúzódást okoznak.
Egy speciális szimpatikus szerv, a mellékvesevelő, amely embrionálisan a ganglionokkal azonos eredetű, közvetlenül a véráramba bocsátja ki a adrenalint (epinefrin) és noradrenalint (norepinefrin). Ezek a hormonok a véráramon keresztül az egész testben elterjednek, és hasonló hatásokat váltanak ki, mint a noradrenalin, de általában erőteljesebbek és tartósabbak, mivel a vérben hosszabb ideig keringenek.
A szimpatikus idegrendszer hatékonyságát a gyors, diffúz és szinte minden szervrendszerre kiterjedő válaszreakciója biztosítja, felkészítve a szervezetet a hirtelen fellépő stresszhelyzetek kezelésére.
A szimpatikus idegrendszer modulálja a vérnyomás szabályozását is. Az erek falában található simaizmok összehúzódásával (vasokonstriktor hatás) növeli a perifériás ellenállást, ami emeli a vérnyomást. Ezzel párhuzamosan a szívizomzat fokozott működése is hozzájárul a vérkeringés gyorsításához. A légutak simaizomzatának ellazítása (bronchodilatáció) pedig növeli az oxigénbeáramlást.
Az adaptációs mechanizmusok részeként a szimpatikus aktivitás befolyásolja az anyagcserét is. Elősegíti a máj glikogénraktárainak lebontását glükózzá, így biztosítva a gyorsan felhasználható energiát az izmok és az agy számára. Ezenkívül a zsírszövetből is mobilizál zsírsavakat.
Az élettani válaszokat az idegrendszeren belül neurotranszmitterek, míg a mellékvesevelőn keresztül hormonok közvetítik. A szimpatikus idegrendszer tehát egy integrált, több szinten működő rendszer, amely a szervezet gyors reagálását teszi lehetővé a külső és belső változásokra.
A szimpatikus idegrendszer működésének molekuláris mechanizmusai
A szimpatikus idegrendszer stresszválaszában a molekuláris szintű mechanizmusok kulcsfontosságúak a gyors és hatékony adaptáció szempontjából. Miután a szimpatikus idegrendszer aktiválódik, az idegvégződésekből felszabaduló neurotranszmitterek, elsősorban a noradrenalin, specifikus receptorokhoz kötődnek a célsejtek felszínén. Ezek a receptorok, az adrenerg receptorok, két fő csoportra oszthatók: alfa (α) és béta (β) receptorokra, amelyek további alcsoportokra tagolódnak (pl. α1, α2, β1, β2, β3). E receptorok kötődése különböző intracelluláris jelátviteli útvonalakat aktivál, amelyek végül a sejt specifikus válaszát váltják ki.
Például a szívizomzatban található β1 adrenerg receptorok aktiválódása adenilát-cikláz enzim termelését fokozza, ami emeli a cAMP (ciklikus adenozin-monofoszfát) szintet. Ez a cAMP pedig protein-kináz A (PKA) aktiválásán keresztül fokozza a kalciumionok beáramlását a szívsejtekbe, ami gyorsabb és erősebb szívveréshez vezet. Ezzel szemben az erek simaizomzatában található α1 adrenerg receptorok aktiválódása foszfolipáz C (PLC) útvonalat indít el, ami növeli a sejten belüli kalciumion-koncentrációt, így az erek összehúzódását (vasokonstrikciót) idézve elő.
A szimpatikus idegrendszer molekuláris szinten a neurotranszmitterek és specifikus receptorok kölcsönhatásán keresztül képes precízen és gyorsan befolyásolni a célsejtek működését, lehetővé téve a szervezet számára a stresszhelyzetekhez való alkalmazkodást.
A mellékvesevelő által termelt adrenalin és noradrenalin is ezekhez az adrenerg receptorokhoz kötődve fejtenek ki hatást, de mivel hormonokként a véráramban terjednek, hatásuk szisztémásabb és tartósabb. Az adrenalin erőteljesebben kötődik a β receptorokhoz, míg a noradrenalinnek nagyobb affinitása van az α receptorokhoz, bár mindkettő mindkét típusú receptorhoz kötődhet.
Az adaptációs folyamat részeként a szimpatikus idegrendszer a glükózanyagcsere mobilizálásában is szerepet játszik. A májban található β2 adrenerg receptorok aktiválódása fokozza a glikogén lebontását glükózzá (glikogenolízis), így növelve a vércukorszintet és biztosítva a gyorsan hozzáférhető energiát. Ezzel párhuzamosan a zsírszövetben található β3 adrenerg receptorok aktiválása elősegíti a zsírok lebontását (lipolízis), további energiaforrásokat biztosítva.
Ezek a molekuláris mechanizmusok biztosítják a szimpatikus idegrendszer által kiváltott komplex élettani válaszok koordinált és hatékony végrehajtását, amelyek létfontosságúak a túlélés szempontjából a fenyegető helyzetekben.
Az „üss vagy fuss” válasz biokémiai és fiziológiai háttere
Az „üss vagy fuss” válasz biokémiai és fiziológiai alapjai a szimpatikus idegrendszer gyors és hatékony működésében rejlenek. Amikor az agy a hypothalamuson keresztül észleli a stresszhelyzetet, azonnali parancsokat küld a szimpatikus idegrendszernek. Ez a parancsok továbbítódnak a gerincvelőn keresztül a szimpatikus dúcokhoz, ahol a neurotranszmitterek, elsősorban az acetilkolin, átkapcsolódnak a posztganglionáris neuronokra.
Ezek a posztganglionáris neuronok aztán a noradrenalint bocsátják ki, amely a célsejteken lévő adrenerg receptorokhoz (alfa és béta) kötődve váltja ki a specifikus élettani válaszokat. Az alfa-receptorok főként az erek simaizmainak összehúzódását okozzák, növelve a vérnyomást és átirányítva a vért a létfontosságú szervek, mint az agy és az izmok felé. Ezzel párhuzamosan a béta-receptorok, különösen a szívben, növelik a szívverés sebességét és erejét, biztosítva a gyorsabb véráramlást.
A szimpatikus idegrendszer másik kulcsfontosságú hatása a mellékvesevelő stimulálása. Ez a mirigy, a szimpatikus idegvégződésekkel szoros kapcsolatban állva, közvetlenül a véráramba bocsátja az adrenalint és a noradrenalint. Ezek a hormonok, a noradrenalinhoz hasonlóan, de általában intenzívebb és tartósabb hatással, fokozzák a szív teljesítményét, növelik a vérnyomást, és serkentik a glükóz felszabadulását a máj glikogénraktáraiból. Ez a hirtelen rendelkezésre álló glükóz kulcsfontosságú az energiát igénylő fizikai aktivitáshoz.
A légutakban a simaizmok ellazulnak, ami bronchodilatációt eredményez, így több oxigén juthat a tüdőbe. A pupillák kitágulása, a mydriasis, javítja a látóteret, lehetővé téve a potenciális veszélyek jobb észlelését. Az emésztőrendszer működése pedig háttérbe szorul, mivel a vér elkerüli a nem sürgős funkciókat, és az energiát a vészhelyzet kezelésére fordítja a szervezet.
A biokémiai és fiziológiai változások komplex együttese teszi lehetővé a szimpatikus idegrendszer „üss vagy fuss” válaszát, amely egy evolúciósan kialakult túlélési mechanizmus.
A stresszválasz ezen fázisában a glükóz és a zsírsavak mobilizálása az elsődleges energiaforrások biztosítása érdekében. A májban tárolt glikogén glükózzá alakul, míg a zsírszövetből felszabaduló zsírsavak is felhasználhatók energiaként. Ez az anyagcsere-változás biztosítja, hogy az izmok és az agy elegendő üzemanyaghoz jussanak a megterhelő helyzet leküzdéséhez.
Az „üss vagy fuss” válasz nem csupán a fizikai reakciókra korlátozódik. A szimpatikus aktiváció befolyásolja az agyi funkciókat is, éberré és koncentráltabbá téve az egyént. A figyelem élesedik, és a döntéshozatal felgyorsul, hogy a lehető leghatékonyabban tudjon reagálni a veszélyre.
Érdekesség, hogy bár a szimpatikus idegrendszer elsősorban a gyors, akcióorientált válaszokat váltja ki, bizonyos esetekben, mint például a hideghez való adaptáció során, a hőtermelés fokozása is szerepet játszik a funkciójában, például a barna zsírszövet aktiválásával.
A stresszhormonok szerepe a szimpatikus idegrendszer aktiválásában
A stresszhormonok, különösen az adrenalin (epinefrin) és a noradrenalin (norepinefrin), kulcsfontosságúak a szimpatikus idegrendszer gyors és hatékony aktiválásában. Ezeket a hormonokat a mellékvesevelő termeli és választja ki közvetlenül a véráramba, miután a szimpatikus idegrendszer impulzusokat kapott. Ez a hormonális válasz kiegészíti és felerősíti az idegi jelátvitelt, biztosítva a szervezet teljes körű felkészítését a stresszhelyzetre.
Az agyban, különösen a hipotalamuszban zajló információfeldolgozás hatására indul el a szimpatikus idegrendszer aktiválása. A hipotalamusz jelzéseket küld a gerincvelőn keresztül a mellékvesevelő felé. Amint a mellékvesevelő megkapja ezeket a szimpatikus idegi impulzusokat, azonnal megkezdi az adrenalin és noradrenalin kibocsátását. Ezek a katekolaminok a véráramba kerülve gyorsan eljutnak a test különböző pontjaira, ahol specifikus adrenerg receptorokhoz kötődnek.
A stresszhormonok, mint az adrenalin és noradrenalin, nem csupán a szimpatikus idegrendszer által közvetített hatásokat erősítik, hanem önmagukban is képesek jelentős élettani változásokat előidézni, globális stresszválaszt generálva.
Az adrenalin és noradrenalin hatása széleskörű. Gyorsítják a szívverést, növelik a vérnyomást, kitágítják a légutakat, és energiát szabadítanak fel a szervezet számára. Például a májban a glikogén lebontását serkentik glükózzá, amely azonnal felhasználható energiaforrássá válik. Ezenkívül fokozzák a zsírraktárak mobilizálását is, további energiaforrást biztosítva.
A hormonális válasz tartósabb hatású lehet, mint a tisztán idegi jelátvitel. Míg az idegi impulzusok rendkívül gyorsak, de viszonylag rövid ideig tartanak, a vérben keringő hormonok hosszabb ideig fejtik ki hatásukat, így a szervezet hosszabb ideig képes fenntartani a fokozott működést a stresszforrás fennállása alatt. Ez a kettős mechanizmus – az idegi és hormonális válasz együttes működése – biztosítja a szimpatikus idegrendszer rugalmasságát és hatékonyságát a különféle stresszhelyzetek kezelésében.
Fontos megérteni, hogy bár ez a válasz evolúciós szempontból rendkívül előnyös volt az emberiség túlélése szempontjából, a modern, krónikus stresszhelyzetekben a stresszhormonok tartósan magas szintje komoly egészségügyi problémákhoz vezethet. A szív- és érrendszeri megbetegedések, valamint az anyagcsere-zavarok gyakran összefüggésbe hozhatók a tartósan aktivált stresszhormonrendszerrel.
Az adaptációs mechanizmusok az akut stresszhelyzetekben
Az akut stresszhelyzetekben a szimpatikus idegrendszer által vezérelt adaptációs mechanizmusok célja a szervezet gyors felkészítése a veszély elhárítására vagy elkerülésére. Ezek a válaszok nemcsak a már említett fiziológiai változásokat (mint a szívverés gyorsulása és a vérnyomás emelkedése) foglalják magukban, hanem magukban foglalnak finomhangolt biokémiai és celluláris folyamatokat is, amelyek a túlélés esélyét maximalizálják.
Az egyik kulcsfontosságú adaptációs lépés a glükóztartalékok mobilizálása. A szimpatikus idegrendszer stimulálja a májat a glikogénraktárak lebontására, hogy glükózt bocsásson a véráramba. Ez a gyorsan hozzáférhető energiaforrás elengedhetetlen az agy és az izmok fokozott működéséhez a stresszhelyzet idején. Emellett a zsírszövetből felszabaduló zsírsavak is hozzájárulnak az energiaszükséglet fedezéséhez, különösen hosszabb ideig tartó megterhelés esetén.
A szimpatikus válasz magában foglalja az immunrendszer átmeneti aktiválását is. Bizonyos immunsejtek, mint a neutrofilok és a természetes ölősejtek (NK-sejtek), mobilizálódnak és a véráramba kerülnek. Ez a kezdeti immunitásfokozódás segíthet a potenciális sérülések vagy fertőzések megelőzésében, amelyek egy fizikai konfrontáció során előfordulhatnak. Azonban a tartósan fennálló stressz ellentétes hatást válthat ki, hozzájárulva az immunrendszer gyengüléséhez.
A szimpatikus idegrendszer által vezérelt adaptációs mechanizmusok egy komplex, összehangolt válaszrendszert alkotnak, amelynek célja a szervezet optimális teljesítményének biztosítása a túlélés szempontjából kritikus helyzetekben.
A légutak tágulása (bronchodilatáció) is fontos adaptációs válasz. A szimpatikus idegrendszer hatására a hörgők simaizmai ellazulnak, megnövelve a légutak keresztmetszetét. Ez lehetővé teszi a nagyobb mennyiségű oxigén beáramlását a tüdőkbe, ami elengedhetetlen a fokozott energiaigény kielégítéséhez. A légzés sekélyebbé és gyorsabbá válása is ezt a célt szolgálja.
A visszajelzési mechanizmusok, mint például a vérnyomás és a vér glükózszintjének monitorozása, folyamatosan szabályozzák a szimpatikus válasz intenzitását. Ezek a visszacsatolások biztosítják, hogy a szervezet ne reagáljon túl, és a stresszhelyzet elmúltával a rendszerek visszatérjenek a homeosztatikus állapotba. Azonban a krónikus stressz megzavarhatja ezeket a szabályozó köröket, ami tartós egészségügyi problémákhoz vezethet.
Az akut stresszhelyzetekben a szimpatikus idegrendszer által elindított adaptációk nem csupán a fizikai túlélésre összpontosítanak, hanem magukban foglalnak olyan kognitív és viselkedésbeli változásokat is, mint az éberség növekedése és a figyelem koncentrációja a fenyegetésre. Ezek a komplex válaszok biztosítják, hogy az egyén a lehető leghatékonyabban tudjon reagálni a váratlan kihívásokra.
A krónikus stressz hatása a szimpatikus idegrendszerre és a homeosztázisra
Míg az akut stresszhelyzetekben a szimpatikus idegrendszer gyors és hatékony válasza az adaptáció kulcsa, a krónikus stressz eltérő és káros következményekkel járhat a szervezet homeosztázisára nézve. Ha a szervezet folyamatosan fenyegetettség alatt áll, a szimpatikus idegrendszer állandósult aktiváltsága megzavarja a vegetatív idegrendszer finom egyensúlyát, amely alapvető a normális élettani működéshez.
Az állandósult szimpatikus túlstimuláció jelensége, amelyet gyakran „stressz betegségek” kialakulásának egyik fő okaként említenek, számos negatív hatást gyakorol a szervezetre. A tartósan magas vérnyomás, amely az erek folyamatos összehúzódásából ered, jelentősen növeli a szív- és érrendszeri betegségek, mint például a szívinfarktus és a stroke kockázatát. A szervezetben felhalmozódó stresszhormonok, mint a kortizol (amelynek termelését a szimpatikus rendszer aktiválása is befolyásolja a hipotalamusz-hipofízis-mellékvese tengelyen keresztül), gyengíthetik az immunrendszert, így a szervezet fogékonyabbá válik a fertőzésekkel és betegségekkel szemben.
A krónikus stressz hatására a szimpatikus idegrendszer túlzott aktivitása megzavarja a szervezet természetes regenerálódási és helyreállítási folyamatait, elősegítve a krónikus betegségek kialakulását és súlyosbodását.
Az emésztőrendszerre gyakorolt hatások is jelentősek. A krónikus stressz gyomor- és bélrendszeri problémákhoz vezethet, mint például fekélyek, irritábilis bél szindróma (IBS) vagy gyulladásos bélbetegségek. A szimpatikus idegrendszer dominanciája csökkenti a gyomor-bél traktus véráramlását és motilitását, ami megnehezíti az emésztést és a tápanyagok felszívódását.
A mentális egészség terén is megfigyelhetők káros következmények. A tartós szimpatikus aktiváció hozzájárulhat a szorongás, a depresszió és a kimerültség (burnout) kialakulásához. Az alvásminták zavarai, az állandó éberség és a nehézkes relaxáció mind a szimpatikus idegrendszer túlműködésének jelei lehetnek.
A homeosztázis fenntartása szempontjából kulcsfontosságú a parasimpatikus idegrendszer szerepének helyreállítása. A paraszimpatikus rendszer felelős a szervezet „pihenés és emésztés” (rest-and-digest) állapotáért, amely ellensúlyozza a szimpatikus aktivitást. Krónikus stressz esetén ez az egyensúly felborul, és a paraszimpatikus hatások csökkennek. A stresszkezelési technikák, mint a meditáció, a légzőgyakorlatok vagy a mindfulness, segíthetnek a paraszimpatikus aktivitás erősítésében és ezáltal a szimpatikus túlstimuláció csökkentésében, elősegítve a szervezet visszatérését az egészséges homeosztázishoz.
Szimpatikus idegrendszeri túlműködés és kapcsolódó betegségek
Amikor a szimpatikus idegrendszer tartósan vagy túlzottan aktívvá válik, az jelentős egészségügyi következményekkel járhat. A krónikus stressz, amelyet modern életünk gyakran generál, folyamatosan fenntartja a „harcolj vagy menekülj” válasz állapotát, még akkor is, ha nincs valós veszély. Ez a persistent szimpatikus aktiváció kardiovaszkuláris problémákhoz vezethet, mint például magas vérnyomás (hipertónia), amely növeli a szívroham és a stroke kockázatát. A megnövekedett szívverés és a fokozott szívizommunka hosszú távon megterheli a szívet.
Az emésztőrendszerre is negatív hatással van a szimpatikus túlműködés. A gyomor- és bélmozgások lelassulása emésztési zavarokhoz, irritábilis bél szindróma (IBS) tüneteihez, vagy akár gyomorfekély kialakulásához is hozzájárulhat, mivel csökken a gyomor és a belek véráramlása, és megváltozik a bélflóra összetétele.
A tartós szimpatikus idegrendszeri túlműködés nem csupán átmeneti kellemetlenségeket okoz, hanem komoly, krónikus betegségek kialakulásának kockázatát is jelentősen növeli.
Az anyagcsere terén is megfigyelhetőek károsodások. A vércukorszint emelkedése, amelyet a glükóz mobilizációja okoz, hosszú távon 2-es típusú diabétesz kialakulásához vagy súlyosbodásához vezethet. A szervezet folyamatosan magas adrenalinszintje megnehezíti a normál anyagcsere-folyamatok fenntartását.
A mentális egészség is súlyosan érintett. A szimpatikus túlstimuláció hozzájárulhat a szorongás, pánikbetegség és depresszió kialakulásához. Az alvászavarok, mint az inszomnia, szintén gyakoriak, mivel a szervezet nehezen tud átkapcsolni a pihenő (parasimpatikus) állapotba. A tartós stressz és a fokozott éberség állapota kimeríti az idegrendszert.
Ezenkívül a krónikus gyulladások és az immunrendszer működésének zavarai is összefüggésbe hozhatók a szimpatikus idegrendszer túlzott aktivitásával. A szervezet folyamatos „készültségi” állapota gyengítheti az immunválasz hatékonyságát, így fogékonyabbá téve a szervezetet a fertőzésekre.
A szimpatikus idegrendszer modulációjának terápiás lehetőségei
A szimpatikus idegrendszer túlzott vagy krónikus aktiválódása számos egészségügyi problémához járulhat hozzá, mint például magas vérnyomás, szív- és érrendszeri betegségek, szorongásos zavarok és alvászavarok. Éppen ezért a szimpatikus idegrendszer modulációjának terápiás lehetőségei kiemelt fontosságúak a modern orvoslásban.
Az egyik fő terápiás stratégia a gyógyszeres beavatkozás. Különböző gyógyszercsoportok képesek befolyásolni a szimpatikus idegrendszer működését. A béta-blokkolók például gátolják a béta-adrenerg receptorok működését, csökkentve ezzel a szívverést és a vérnyomást, és így mérsékelve a szimpatikus aktivitás káros hatásait. Az alfa-blokkolók hasonlóan, az alfa-receptorok blokkolásával érik el az érfal ellazítását és a vérnyomás csökkentését. Egyes vérnyomáscsökkentők, mint például az ACE-gátlók és az angiotenzin II receptorblokkolók, indirect módon is csökkenthetik a szimpatikus tónust, mivel befolyásolják a rennin-angiotenzin-aldoszteron rendszert, amely szorosan összefonódik az autonóm idegrendszerrel.
A viselkedésterápiák és relaxációs technikák is hatékonyan segíthetnek a szimpatikus túlstimuláció kezelésében. A meditáció, a progresszív izomrelaxáció, a jóga és a légzéstechnikák révén az egyének megtanulhatják tudatosan befolyásolni vegetatív válaszaikat, elősegítve a paraszimpatikus idegrendszer dominanciáját és csökkentve a stresszhormonok szintjét. Ezek a módszerek segítik a szervezet visszatérését a homeosztázishoz, csökkentve a szimpatikus „harcolj vagy menekülj” válasz tartós fennállását.
A szimpatikus idegrendszer modulációjának célja a túlzott aktiváció mérséklése, a paraszimpatikus rendszer erősítése és a szervezet általános stressztűrő képességének növelése.
A fizikai aktivitás, különösen a rendszeres, mérsékelt intenzitású mozgás, szintén pozitív hatással van a vegetatív idegrendszer egyensúlyára. Bár a testmozgás kezdetben növeli a szimpatikus aktivitást, a rendszeres edzés hosszú távon javítja az autonóm idegrendszer rugalmasságát és válaszkészségét, csökkentve a krónikus stressz negatív hatásait.
Egyes speciális esetekben, mint például súlyos poszttraumás stressz zavar (PTSD) vagy krónikus fájdalom szindrómák esetén, idegblokádok vagy idegstimulációs technikák is szóba jöhetnek. Ezek célzottan befolyásolják az idegsejtek jelátvitelét, megcélozva a szimpatikus idegrendszer azon részeit, amelyek túlzott aktivitást mutatnak.
Az élettani változások megértése, beleértve a neurotranszmitterek és hormonok szerepét, lehetővé teszi az orvosok számára a célzott terápiás stratégiák kidolgozását. A klinikai pszichológia és a pszichiátria is kulcsszerepet játszik a stresszkezelésben, segítve a betegeket a stresszorok azonosításában és hatékony megküzdési stratégiák kialakításában.