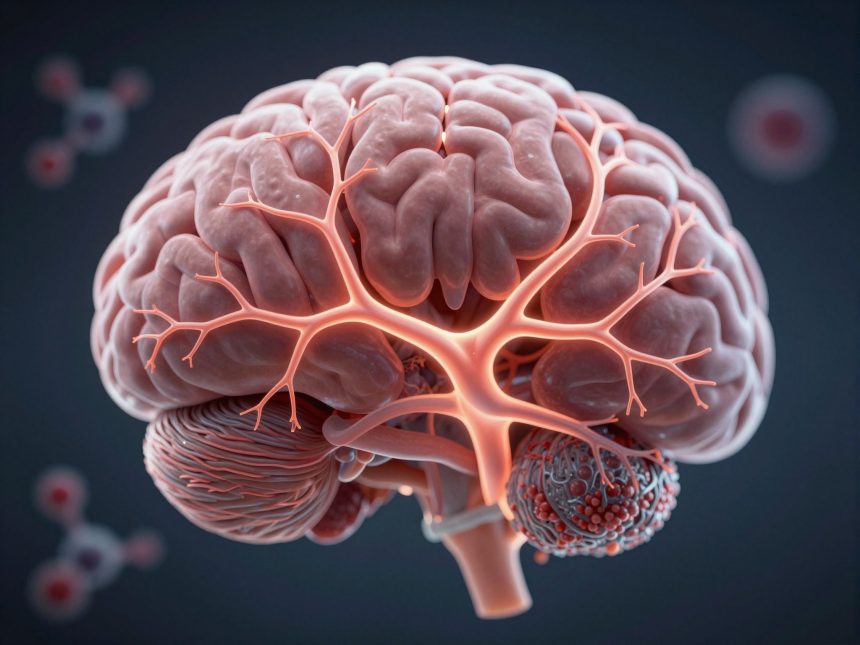
Az agy rendkívül érzékeny szerv, amelynek optimális működéséhez szigorú belső környezetre van szükség. A vér-agy gát (VAG) egy komplex biológiai struktúra, amely elengedhetetlenül fontos az agy védelmében és a neurológiai egészség fenntartásában. Ez a speciális barrier megakadályozza, hogy a vérben található káros anyagok, például toxinok, kórokozók és gyógyszerek bejussanak az agysejtekhez.
A VAG fő alkotóelemei az endothel sejtek, amelyek a kapillárisok belső falát bélelik. Ezek az endothel sejtek szorosan kapcsolódnak egymáshoz, így minimális intercelluláris rést hagynak. Ez a szoros kapcsolódás jelenti a VAG elsődleges fizikai akadályát. Ezen kívül, a VAG tartalmaz pericitákat és asztrocitákat, amelyek tovább erősítik a gát szerkezetét és funkcióját, aktívan részt vesznek a tápanyagok szállításában és a méreganyagok eltávolításában.
A vér-agy gát hatékonyan szűri a vérből érkező anyagokat, biztosítva az agy számára a kiegyensúlyozott és biztonságos környezetet.
A VAG szelektív permeabilitása alapvető a toxinszűrés szempontjából. Bizonyos molekulák, mint az oxigén és a glükóz, könnyen átjutnak a VAG-n, hogy táplálják az agyat. Ezzel szemben a nagyobb méretű vagy elektromos töltéssel rendelkező anyagok, valamint a vízben rosszul oldódó molekulák átjutása jelentősen korlátozott. Ez a szelekció aktív transzport mechanizmusokon keresztül valósul meg, amelyek specifikusan irányítják a szükséges anyagok bejutását, miközben kizárják a potenciálisan károsakat.
A VAG működésének megértése kulcsfontosságú a különböző neurológiai betegségek, mint például az Alzheimer-kór, a Parkinson-kór és az agyhártyagyulladás kezelésének és megelőzésének szempontjából. A gát sérülése vagy megváltozott működése hozzájárulhat ezeknek a kórképeknek a kialakulásához és progressziójához. A VAG integritásának megőrzése, valamint a károsodott gát helyreállítása jelentős kutatási terület a neurológiai terápiák fejlesztésében.
A Vér-agy Gát Anatómiai és Molekuláris Szerkezete
A vér-agy gát (VAG) anatómiai és molekuláris felépítése egyedülálló specializációt mutat, amely lehetővé teszi a központi idegrendszer (KIR) számára a külső hatásoktól való hatékony elszigetelődését. Míg az eddigiekben említettük az endothel sejtek szoros kapcsolódásait, a VAG szerkezetét ennél sokkal komplexebb molekuláris mechanizmusok is alkotják. Az endothel sejtek közötti tight junction (szoros kapcsolódás) komplexek kulcsfontosságúak. Ezek a több fehérjekomponensből álló struktúrák, mint például a claudinok és az occludinek, gyakorlatilag leplombálják az intercelluláris réseket, megakadályozva az anyagok parasejtes transzportját. Ez a molekuláris „zár” biztosítja a VAG magas elektromos ellenállását, ami jelzi a szoros sejtkapcsolódást.
Az endothel sejtek felszínén található specifikus transzporter fehérjék is elengedhetetlen részei a VAG-nak. Ezek a molekulák aktív transzport révén teszik lehetővé létfontosságú tápanyagok, mint például a glükóz (a GLUT1 transzporter segítségével) és az aminosavak bejutását az agyba. Ugyanakkor ezek a transzporterek, valamint a efflux pumpák (például az ABC transzporterek családja), képesek eltávolítani bizonyos toxinokat vagy gyógyszereket a KIR-ből, ezzel is hozzájárulva a toxinszűréshez. A VAG nem csupán egy passzív barrier, hanem egy dinamikus, aktívan szabályozott struktúra.
A VAG-t alkotó mikrovaszkuláris egység magában foglalja az endothel sejtek mellett az említett pericitákat és asztrocitákat is. Az asztrociták lábnyúlványai szorosan körülölelik a kapillárisokat, és jelátviteli molekulák kibocsátásával befolyásolják az endothel sejtek működését, beleértve a tight junction-ök kialakulását és fenntartását. Ezen sejtek együttes működése biztosítja a VAG strukturális integritását és funkcionális épségét.
A vér-agy gát molekuláris komplexitása és a sejtek közötti szoros együttműködés garantálja az agy szelektív védelmét és a káros anyagok hatékony kiszűrését.
A VAG lipofil (zsírban oldódó) anyagok számára viszonylag könnyű átjutást biztosít, míg a hidrofil (vízben oldódó), különösen az ionos vegyületek átjutását erősen korlátozza. Ez a tulajdonság fontos a gyógyszerfejlesztés szempontjából, mivel a hatóanyagok VAG-n való átjutásának képessége jelentősen befolyásolja azok hatékonyságát neurológiai megbetegedések esetén. A VAG sejtes és molekuláris szintű felépítése teszi lehetővé az agy számára a belső homeosztázis fenntartását, ami elengedhetetlen a normál neurológiai működéshez és a károsodások elkerüléséhez.
A Vér-agy Gát Funkciói: Toxinok Kirekesztése és Tápanyagok Bevitele
A vér-agy gát (VAG) kettős funkciót lát el az agy egészségének védelmében: szelektíven beengedi a létfontosságú tápanyagokat, miközben aktívan kirekeszti a káros anyagokat. Ez a kettős működés biztosítja az agy optimális működését és a neurológiai károsodások megelőzését. A tápanyagok bevitele nem véletlenszerű; speciális transzporter fehérjék felelősek a szükséges molekulák, mint például a glükóz és az esszenciális aminosavak célzott szállításáért az agysejtekhez. Ez a precíz mechanizmus garantálja, hogy az agy folyamatosan hozzájuthasson az energiaszükségletéhez és a felépítéséhez szükséges építőkövekhez.
Ezzel párhuzamosan a VAG komplex szűrőrendszert működtet a toxinok ellen. Nem csupán passzívan blokkolja a káros vegyületeket, hanem aktív efflux mechanizmusokkal is rendelkezik, amelyek képesek eltávolítani azokat az agyszövetből, mielőtt azok jelentős kárt okozhatnának. Ezek az efflux pumpák, mint például az ABC transzporterek, kulcsfontosságúak a neurotoxinok, a metabolikus melléktermékek és bizonyos idegen anyagok, például gyógyszerek eltávolításában. A VAG hatékonysága ezen a téren elengedhetetlen a neurológiai egészség megőrzéséhez, különösen olyan helyzetekben, amikor a szervezet toxikus terhelésnek van kitéve.
A vér-agy gát nem csupán egy fizikai akadály, hanem egy dinamikus, aktívan szabályozott kapu, amely gondoskodik az agy táplálásáról és védelméről egyidejűleg.
A VAG membrán transzporterek hálózata teszi lehetővé a specifikus tápanyagok, például a ketonok és bizonyos vitaminok bejutását is, amelyek az agy alternatív energiaforrásaiként vagy koenzimekként szolgálnak. Ezen transzporterek szabályozása kulcsfontosságú az agy energia- és tápanyagellátásának finomhangolásához. Ugyanakkor a VAG képes különbséget tenni a jótékony és a káros lipofil molekulák között is, bár ez a folyamat összetettebb, mint a hidrofil vegyületek esetében. A VAG integritásának megőrzése, különösen az öregedés során vagy betegségek hatására bekövetkező változások esetén, kritikus fontosságú a toxinok bejutásának megakadályozására és a normál agyműködés fenntartására.
A VAG toxinszűrési képessége különösen fontos a fejlődő agy számára a magzati és csecsemőkorban. Ebben az életszakaszban a VAG még fejlődésben van, és sérülékenyebb lehet a károsító hatásokkal szemben. A VAG megváltozott permeabilitása, ami például gyulladás vagy fertőzés következtében alakulhat ki, hozzájárulhat olyan neurológiai problémákhoz, mint az agyödéma vagy a neurodegeneratív folyamatok felgyorsulása. Ezért a VAG funkcionális épségének biztosítása alapvető a hosszú távú neurológiai egészség szempontjából.
A Vér-agy Gát Sejtjei: Endothelsejtek, Periciták és Asztrociták Szerepe
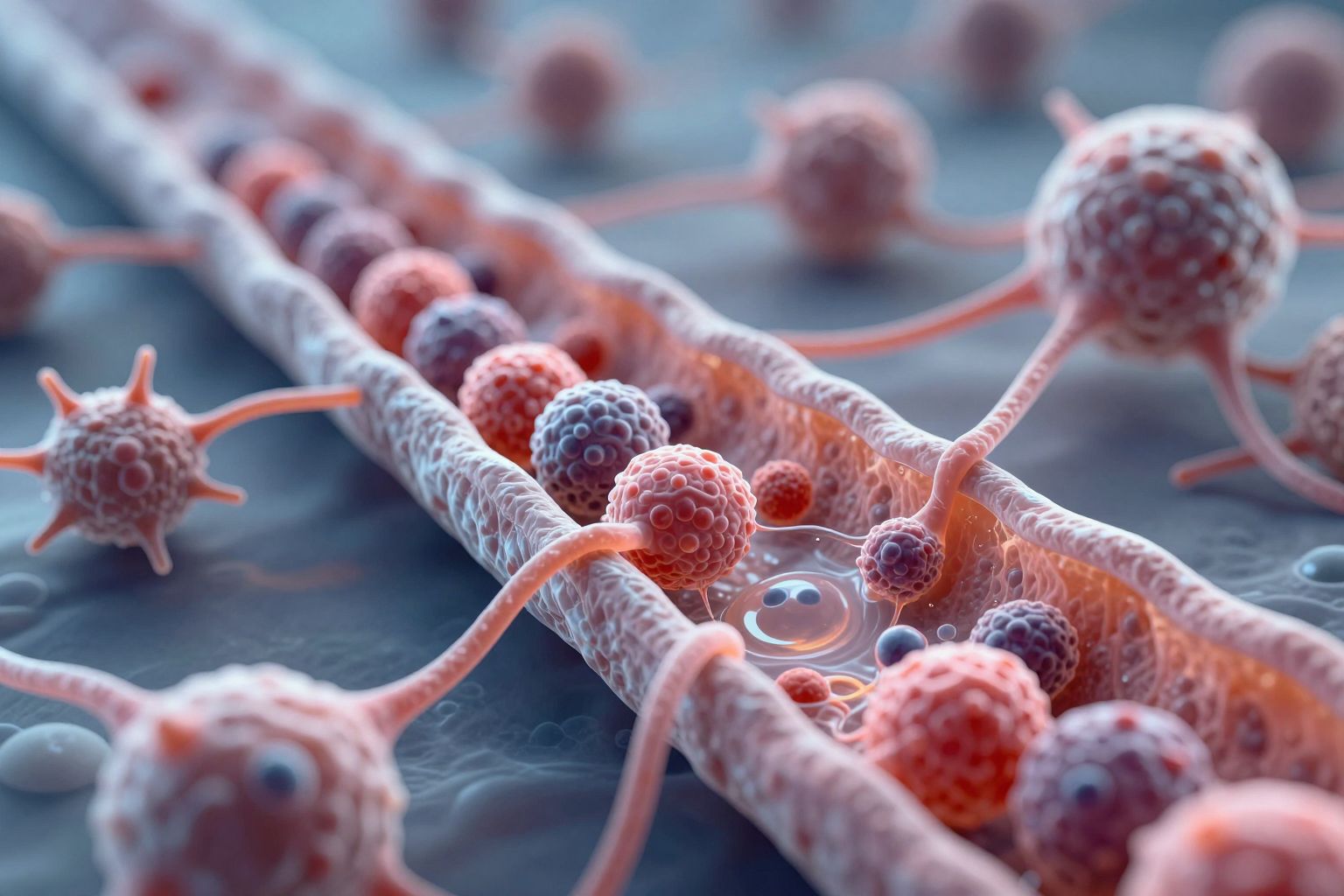
A vér-agy gát (VAG) három fő sejttípus szoros együttműködésén keresztül biztosítja az agy védelmét és a toxinszűrés hatékonyságát. Ezek az endothel sejtek, a periciták és az asztrociták, melyek együttesen alkotják a neurovaszkuláris egységet. Az endothel sejtek, ahogy korábban említettük, a kapillárisok belső falát bélelik, és a köztük lévő szoros kapcsolódások (tight junction-ök) adják a VAG elsődleges fizikai és molekuláris akadályát. Azonban a periciták és az asztrociták jelenléte és aktív szerepe teszi teljessé ezt a védelmi rendszert.
A periciták a kapillárisok falát kívülről borító, speciális sejtek. Ezek az endothel sejtekkel szoros kapcsolatban állnak, és a VAG strukturális integritásának fenntartásában játszanak kulcsszerepet. A periciták szabályozzák az endothel sejtek növekedését és differenciálódását, valamint befolyásolják a tight junction-ök kialakulását és stabilitását. Ezen felül a periciták maguk is képesek szabályozni a véráramlást a kapillárisokban, így hozzájárulva az agy vérellátásának optimális szinten tartásához. Jelenlétük tovább erősíti a VAG permeabilitását szabályozó képességét, megakadályozva az illetéktelen anyagok bejutását.
Az asztrociták a KIR leggyakoribb gliasejtjei, melyek speciális lábnyúlványokkal (pedikelumokkal) szorosan beburkolják a vér-agy gát kapillárisait. Ez a szoros kapcsolat lehetővé teszi az asztrociták számára, hogy közvetlen kommunikációt folytassanak az endothel sejtekkel. Az asztrociták által kibocsátott különböző növekedési faktorok és szignálmolekulák stimulálják az endothel sejteket a tight junction-ök fokozott expressziójára, ezáltal erősítve a VAG barrier funkcióját. Emellett az asztrociták aktívan részt vesznek a neurotranszmitterek metabolizmusában és ionháztartásának szabályozásában az agy extracellularis terében, ami közvetve hozzájárul az agy környezetének stabilitásához.
Az asztrociták és periciták együttesen alkotják az úgynevezett neurovaszkuláris egységet. Ez az egység nem csupán egy fizikai akadályt képez, hanem egy dinamikus, kommunikáló rendszert, amely folyamatosan figyeli és szabályozza az agy belső környezetét. A neurovaszkuláris egység képes reagálni a helyi metabolikus igényekre, például megnövelni a véráramlást bizonyos agyi területeken, ha azok fokozott aktivitást mutatnak. Ezzel párhuzamosan a rendszer felügyeli a potenciálisan káros anyagok jelenlétét a vérben, és aktívan részt vesz azok eltávolításában vagy kiszűrésében.
Az endothel sejtek, periciták és asztrociták szimbiotikus együttműködése biztosítja az agy számára a kritikus védelmet a vérből érkező potenciálisan káros anyagokkal szemben, miközben létfontosságú tápanyagok és oxigén bejutását is lehetővé teszi.
A periciták és asztrociták szerepe különösen fontossá válik olyan neurológiai betegségek esetén, ahol a VAG integritása sérül. Például gyulladásos folyamatok vagy traumák hatására a tight junction-ök lazulhatnak, ami fokozott permeabilitáshoz vezet. Ebben a helyzetben a periciták és asztrociták szabályozó és helyreállító mechanizmusai kulcsfontosságúak lehetnek a VAG funkciójának visszaállításában és az agy további károsodásának megelőzésében. A sejtek közötti jelátviteli útvonalak megértése és manipulálása új terápiás lehetőségeket nyithat meg a neurológiai betegségek kezelésében.
A Vér-agy Gát Áteresztőképességének Szabályozása: Aktív és Passzív Transzportmechanizmusok
A vér-agy gát (VAG) áteresztőképességének szabályozása két fő mechanizmuson alapul: az aktív transzporton és a passzív diffúzió útján történő transzporton. Míg az endothel sejtek szoros kapcsolódásai, az úgynevezett tight junction-ök, fizikai akadályt képeznek a sejtek közötti (parasejtes) útvonalon, a transzcelluláris útvonalat, azaz a sejteken átvezető transzportot, specifikus fehérjék szabályozzák. Ezek a transzporterek teszik lehetővé a létfontosságú molekulák szelektív bejutását az agyba, miközben a káros anyagok belépését korlátozzák.
Az aktív transzport kulcsfontosságú a tápanyagok, mint például a glükóz, bejutásában az agyba. A GLUT1 glükóz transzporter, amely az endothel sejtek membránjában található, nagy affinitással köti meg a glükózt a vérből, és átjuttatja azt a sejten keresztül az agyi extracelluláris térbe. Ez a folyamat energiaigényes, és biztosítja, hogy az agy folyamatosan hozzáférjen a működéséhez elengedhetetlen üzemanyaghoz. Hasonló aktív transzport mechanizmusok felelősek az aminosavak, nukleozidok és bizonyos vitaminok bejutásáért is.
A passzív diffúzió a VAG-n keresztül történő transzport másik jelentős módja. Ez a mechanizmus főként a lipofil (zsírban oldódó) molekulák esetében hatékony. Az ilyen molekulák, mint például az oxigén, a szén-dioxid és bizonyos gyógyszerek, könnyen át tudnak hatolni az endothel sejtek lipid kettősrétegén. A VAG magas lipidtartalma elősegíti ezeknek a molekuláknak a gyors diffúzióját. Ezzel szemben a hidrofil (vízben oldódó) és különösen az ionos vegyületek passzív diffúziója jelentősen korlátozott.
Az aktív és passzív transzport mechanizmusok precíz szabályozása biztosítja az agy szelektív táplálását és a káros anyagok hatékony kiszűrését, fenntartva ezzel a neurológiai egészséget.
Emellett léteznek facilitált diffúziós mechanizmusok is, amelyek nem igényelnek energiát, de specifikus transzporter fehérjéket használnak. Ilyenek például a bizonyos ionok és kis molekulák átjutását segítő csatornák. A VAG-n található efflux pumpák, mint az ABC transzporterek családja, különösen fontosak a toxinszűrésben. Ezek a pumpák aktívan kilökik a káros anyagokat, metabolitokat és bizonyos gyógyszereket a véráramba, megakadályozva azok felhalmozódását az agyban. Ez a dinamikus „szivattyúzó” funkció alapvető a VAG védekező képességében.
A VAG áteresztőképességének szabályozása nem statikus; dinamikus folyamat, amelyet számos faktor befolyásolhat, beleértve a vérnyomást, a gyulladásos folyamatokat és bizonyos hormonális hatásokat. Az idegi aktivitás is szerepet játszik a transzporterek aktivitásának szabályozásában, lehetővé téve az agy energia- és tápanyagigényéhez való alkalmazkodást. A transzporterek és efflux pumpák együttes működése teszi lehetővé az agy számára a homeosztázis fenntartását, biztosítva a megfelelő neurológiai funkciókat és védve a központi idegrendszert a potenciálisan káros külső és belső tényezőktől.
A Vér-agy Gát Sérülése és Megbomlása: Okok és Következmények
A vér-agy gát (VAG) integritásának megőrzése alapvető a neurológiai egészség szempontjából. Azonban számos tényező vezethet a VAG sérüléséhez vagy teljes megbomlásához. Ezek az okok sokrétűek lehetnek, és közvetlenül befolyásolják az agy toxinszűrési képességét, valamint növelik a káros anyagok bejutásának kockázatát. Az egyik leggyakoribb kiváltó ok az agy sérülése, legyen az traumás eredetű (például koponyasérülés) vagy más jellegű károsodás, mint az agyi stroke. Ilyen esetekben a mechanikai vagy keringési zavarok gyulladásos folyamatokat indíthatnak el, amelyek bontják a szoros sejtkapcsolatokat.
A gyulladásos folyamatok általában is jelentős szerepet játszanak a VAG sérülésében. Különböző betegségek, mint például az autoimmun kórképek (pl. szklerózis multiplex), vagy akár egy egyszerű fertőzés is kiválthatnak olyan immunválaszt, amely károsítja a VAG szerkezetét. A gyulladás során felszabaduló citokinek és más gyulladáskeltő molekulák lebontják a tight junction-öket, növelve a permeabilitást. Hasonló hatást fejthetnek ki bizonyos vírusok és baktériumok is, amelyek képesek közvetlenül is megtámadni a VAG sejtes elemeit.
A neurológiai degeneratív betegségek, mint az Alzheimer-kór és a Parkinson-kór is összefüggésbe hozhatók a VAG megváltozott működésével. Bár a pontos mechanizmusok még kutatás tárgyát képezik, feltételezik, hogy a betegségek során felhalmozódó abnormális fehérjék (pl. béta-amiloid) gyulladást keltenek és közvetlenül károsítják a VAG-t. Ez egy ördögi kört hozhat létre: a VAG sérülése elősegíti a káros anyagok agyba jutását, ami tovább súlyosbítja a degeneratív folyamatot.
A rendszertelen táplálkozás, az oxidatív stressz és a magas vérnyomás szintén hozzájárulhatnak a VAG gyengüléséhez. Az oxidatív stressz károsítja a sejteket, beleértve a VAG endothel sejtjeit is, míg a tartósan magas vérnyomás fokozott nyomást gyakorol a kis erekre, ami idővel károsodáshoz vezethet. Ezen kívül, bizonyos toxinok, mint például a nehézfémek vagy a környezeti szennyező anyagok, képesek felhalmozódni a szervezetben és célzottan károsítani a VAG-t.
A vér-agy gát megbomlása megnyitja az utat a potenciálisan neurotoxikus anyagok előtt, ami súlyos következményekkel járhat az agy működésére nézve.
A VAG sérülésének következményei közvetlenül érintik az agy normális működését. Amikor a gát áteresztőképessége megnő, olyan anyagok juthatnak be az agyba, amelyek normál esetben nem tudnának átjutni. Ez agyödémához, idegsejt-károsodáshoz és az agyban zajló gyulladásos folyamatok fokozódásához vezethet. A toxinszűrés hatékonyságának csökkenése pedig tovább terheli az agyat, rontva annak képességét a homeosztázis fenntartására. A VAG integritásának elvesztése neurológiai tünetek széles skáláját válthatja ki, a fejfájástól és memóriazavaroktól kezdve egészen a súlyosabb idegrendszeri betegségek kialakulásáig.
A Vér-agy Gát Megbomlásának Neurológiai Betegségekben Betöltött Szerepe (Alzheimer-kór, Parkinson-kór, MS)
A vér-agy gát (VAG) integritásának megromlása közvetlenül hozzájárulhat számos neurodegeneratív betegség, mint az Alzheimer-kór, a Parkinson-kór és a szklerózis multiplex (SM) kialakulásához és progressziójához. Ezekben a kórképekben a gát sejtes és molekuláris szintű felépítésének sérülése megnöveli a vérből az agyba jutó káros anyagok mennyiségét. Például Alzheimer-kór esetén feltételezik, hogy a VAG diszfunkciója elősegíti az abnormális fehérjék (például béta-amiloid) felhalmozódását az agyszövetben, ami gyulladást és sejtelhalást okoz.
Parkinson-kórban a VAG megváltozott permeabilitása lehetővé teheti toxikus vegyületek bejutását, amelyek károsíthatják a dopaminerg neuronokat, ezáltal súlyosbítva a motoros tüneteket. Szklerózis multiplex esetén a VAG gyulladása és sérülése immunsejtek belépését teszi lehetővé az agyba, ahol gyulladásos folyamatokat indítanak el, károsítva a mielinhüvelyt és az idegrostokat. Ez a jelenség vezet a jellegzetes neurológiai tünetekhez, mint a látászavarok, mozgásképtelenség vagy zsibbadás.
A vér-agy gát megbomlása kritikus tényező lehet a neurodegeneratív betegségek patogenezisében, lehetővé téve a káros anyagok bejutását és az agysejtek gyulladását.
Az eddig említett tight junction komplexek és transzporter fehérjék sérülése vagy diszfunkciója kulcsfontosságú a VAG integritásának elvesztésében. Bizonyos betegségekben a gyulladásos citokinek és a neurotoxinok képesek lebontani ezeket a szerkezeteket, növelve a gát átjárhatóságát. Ezen kívül, a VAG-t alkotó asztrociták és periciták normál működésének zavara is hozzájárulhat a gát gyengeségéhez. A toxinszűrés hatékonyságának csökkenése pedig felgyorsítja az agy károsodását.
A VAG megbomlásának mértékét és jellegét különböző képalkotó eljárásokkal, például kontrasztanyagos MRI-vel lehet vizsgálni. Ezek a vizsgálatok segítenek azonosítani a sérült területeket és követni a betegség progresszióját. A VAG helyreállítására irányuló terápiák, bár még kutatási fázisban vannak, nagy reményeket fűznek a neurodegeneratív betegségek kezeléséhez. A cél az, hogy a VAG újra képes legyen hatékonyan szűrni a vérből érkező anyagokat, minimalizálva az agy károsodását.
A Vér-agy Gát Védelmének Módszerei és Jövőbeli Kutatási Irányok
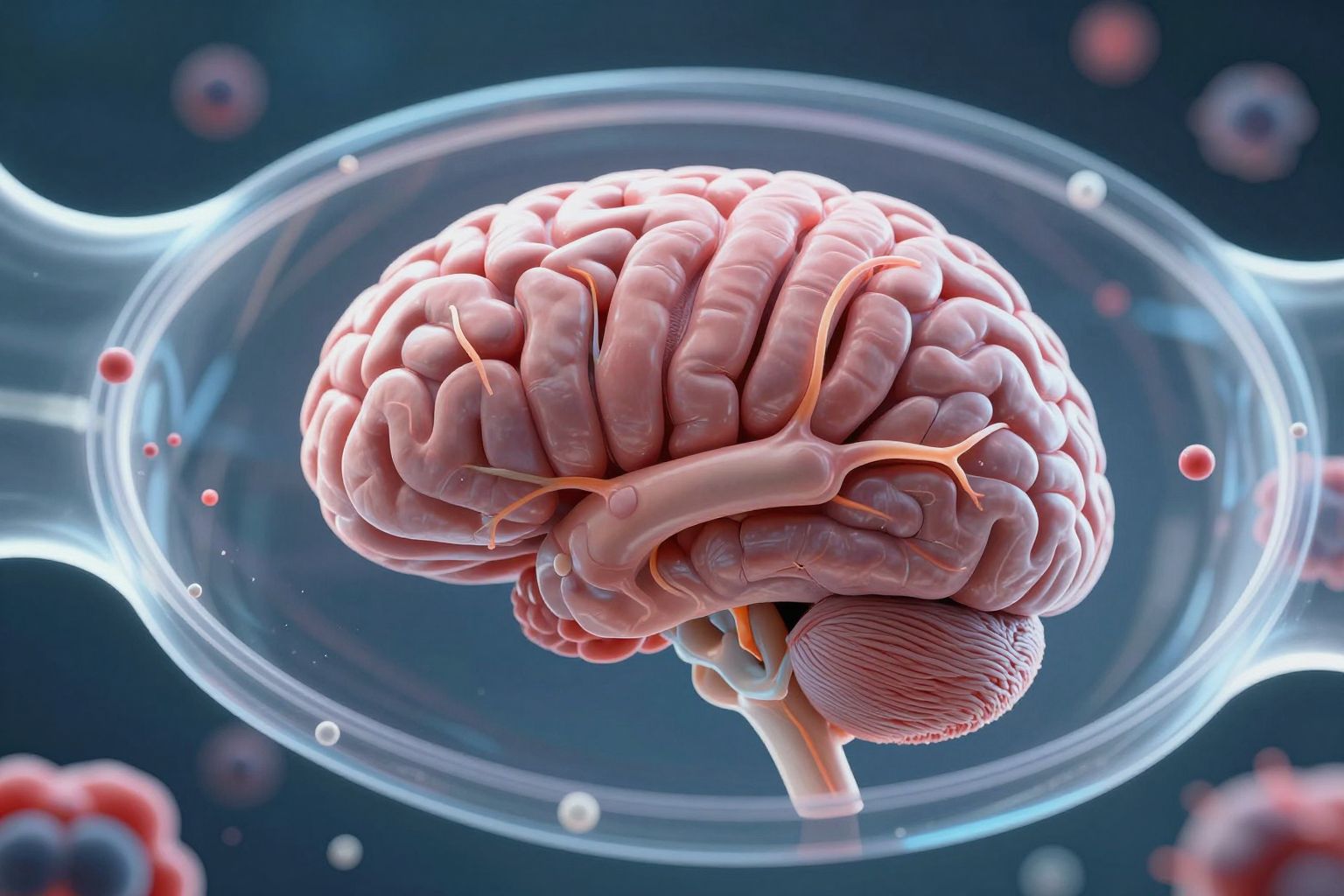
A vér-agy gát (VAG) védelmi mechanizmusainak megértése elengedhetetlen a neurológiai egészség megőrzéséhez és a toxinszűrés hatékony működéséhez. A VAG integritásának fenntartása érdekében különböző terápiás stratégiákat vizsgálnak, amelyek célja a sérült gát helyreállítása vagy a potenciális károsodások megelőzése. Ide tartoznak például a neuroprotektív gyógyszerek, amelyek csökkenthetik a gyulladást és az oxidatív stresszt az agyban, ezáltal közvetve védve a VAG-t.
A jövőbeli kutatások egyik ígéretes területe a célzott gyógyszerbevitel (drug delivery) módszereinek fejlesztése. Mivel a VAG jelentősen korlátozza sok gyógyszer bejutását az agyba, az olyan technikák, mint a nanopartikulumok vagy az ultrahangos módszerek, segíthetnek a hatóanyagok szelektív és hatékony átjuttatásában a VAG-n keresztül. Ez forradalmasíthatja az olyan agyi betegségek kezelését, mint a daganatok vagy az autoimmun idegrendszeri kórképek.
A VAG funkcióinak mélyebb megismerése és az innovatív terápiás megközelítések lehetővé teszik a neurológiai betegségek hatékonyabb kezelését és az agy hosszú távú védelmét.
Emellett a genetikai és molekuláris kutatások is előrelépést ígérnek. Azonosítva a VAG működésében szerepet játszó specifikus géneket és fehérjéket, lehetőség nyílhat a VAG-t szabályozó mechanizmusok befolyásolására. Ezen ismeretek birtokában egyénre szabott terápiák is kifejleszthetők lennének, figyelembe véve az egyén genetikai hajlamait és a VAG állapotát. A mikrobiom és az agy közötti kapcsolat feltárása is új távlatokat nyit a VAG egészségének megőrzésében.